Los virus de las bacterias
El uso de fagos contra la resistencia bacteriana a antibióticos
Introducción a los fagos
Los microorganismos y la humanidad han convivido desde que se originó nuestra especie, hecho que ha dado lugar a interacciones tanto buenas como malas. Muchos microorganismos son beneficiosos para el ser humano, mientras que otros pueden generar enfermedades. Entre los microorganismos más conocidos, encontramos las bacterias y los virus. A diferencia de las bacterias, organismos unicelulares procariotas, los virus son parásitos intracelulares obligados, lo que significa que necesitan de un hospedador para completar su ciclo vital. Están constituidos por ácidos nucleicos que forman su genoma y proteínas que lo recubren. Inertes en el medio extracelular, son capaces de reconocer de forma muy específica a sus hospedadores. Una vez se produce el reconocimiento, inyectan su material genético (es decir, su genoma) en el hospedador, y secuestran su maquinaria celular para poder replicarse y producir progenie viral. En general, existen virus capaces de infectar organismos de los tres dominios de la vida –bacterias, arqueas y eucariotas– y, de hecho, son altamente específicos: cada virus está especializado en reconocer un pequeño rango de hospedadores. Por ejemplo, los virus que infectan bacterias, denominados bacteriófagos, solamente reconocen algunas bacterias, y no podrán reconocer ni infectar nunca células eucariotas. Dentro de los virus de eucariotas, los virus de plantas son muy diferentes de los virus de animales, y dentro de los animales, habrá virus que infecten un tipo celular u otro.
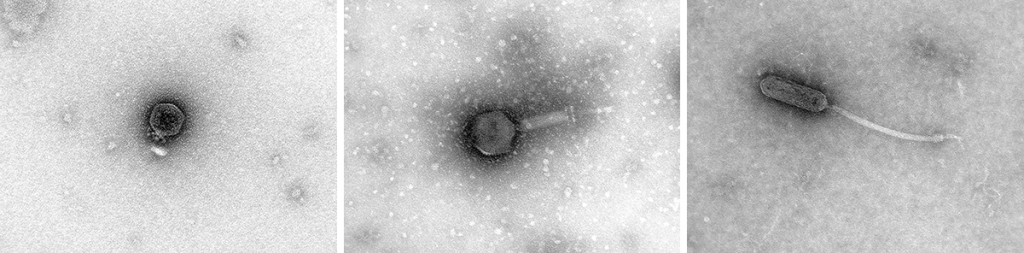
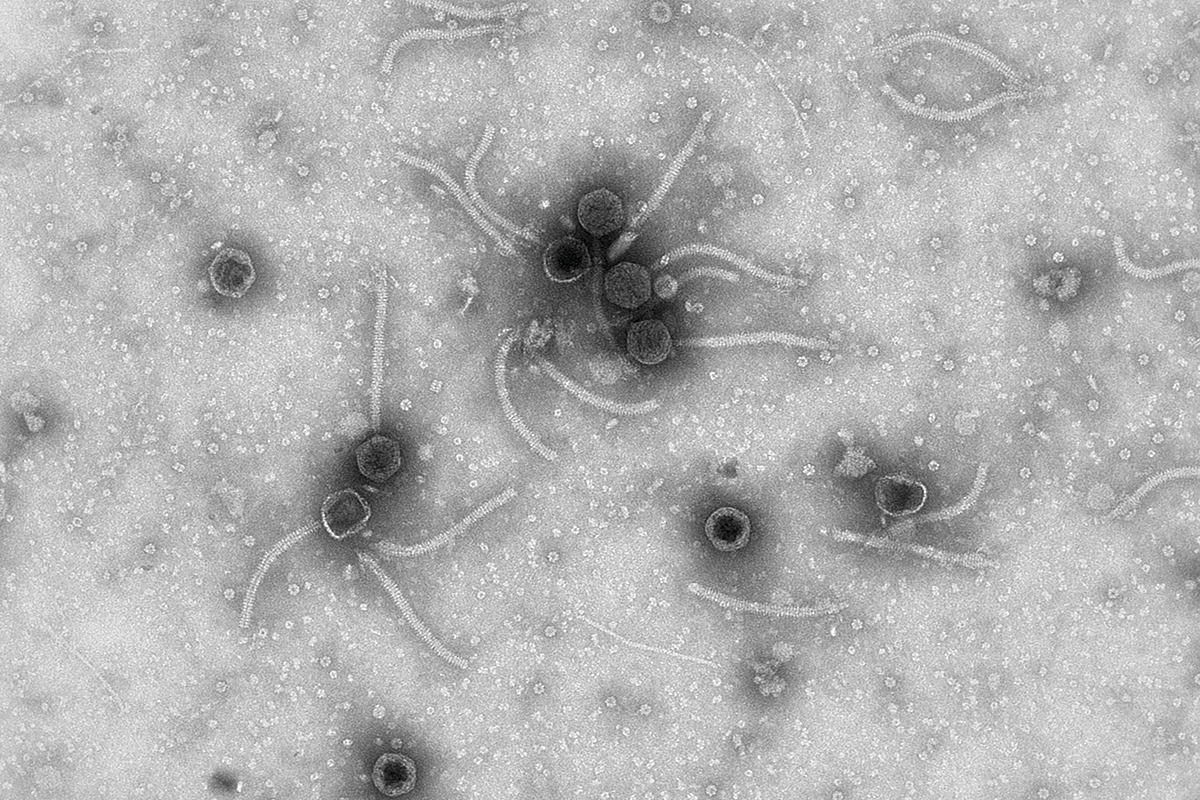
Figura 1. Ejemplos de micrografías de fagos, virus de bacterias, en las que podemos observar su diversidad morfológica. Estas micrografías han sido obtenidas en el Laboratorio de Virología Ambiental y Biomédica del Instituto de Biología Integrativa de Sistemas (UV-CSIC)/ Pilar Domingo-Calap
Los bacteriófagos, o comúnmente llamados fagos, son los virus más abundantes de la biosfera. Se estima que hay 1031 partículas virales, es decir, diez veces más de virus que de bacterias, y que, para cada bacteria, hay al menos un fago capaz de infectarla. Estos números reflejan la importancia de los fagos en los ecosistemas, así como la enorme diversidad que presentan, todavía desconocida. Los fagos contienen genomas que pueden ser de ARN o ADN, de cadena sencilla o doble, circulares o lineales, segmentadas o no segmentadas. Además, se ha observado un gran número de morfologías, que va creciendo conforme se van descubriendo nuevos fagos (Figura 1).
Según su ciclo biológico, los fagos pueden dividirse en fagos líticos y atemperados, aunque se han descrito ciclos alternativos. Los primeros destruyen la bacteria hospedadora en un proceso conocido como lisis, que supone la ruptura de la membrana celular y la liberación del virus al medio extracelular. Los fagos atemperados incorporan su genoma en el del hospedador y se mantienen latentes en forma de profagos, y juegan un papel fundamental en la transferencia horizontal de genes, es decir, la transmisión de información genética entre organismos que no se produce a través de la transmisión vertical.
El descubrimiento de los fagos y sus primeras aplicaciones
Los fagos fueron descubiertos hace ya más de un siglo de manera independiente por el bacteriólogo Frederick Twort (1915) y el microbiólogo Félix d’Hérelle (1917). Ambos buscaban una explicación del halo que a veces observaban cuando hacían cultivos bacterianos en placas de agar (Figura 2). Sin embargo, fue D’Hérelle quien propuso que el halo observado era el resultado de la lisis bacteriana debida a otro microorganismo, al que denominó bacteriófago. D’Hérelle fue también pionero en aplicar los fagos como tratamiento en niños con disentería en Francia y cólera en India, hecho que marca el inicio, por tanto, de la terapia de fagos. Poco después, debido al descubrimiento de la penicilina en 1928 por Alexander Fleming y tras la II Guerra Mundial, el uso de antibióticos de amplio espectro se extendió en los países de Occidente y la terapia de fagos quedó olvidada. Mientras, en los países del Este, donde el acceso a los antibióticos era prácticamente nulo, los fagos continuaron usándose como tratamiento contra infecciones bacterianas, lo que ha favorecido que hoy en día se encuentren allí centros de referencia mundial que siguen utilizando estas terapias de forma rutinaria.
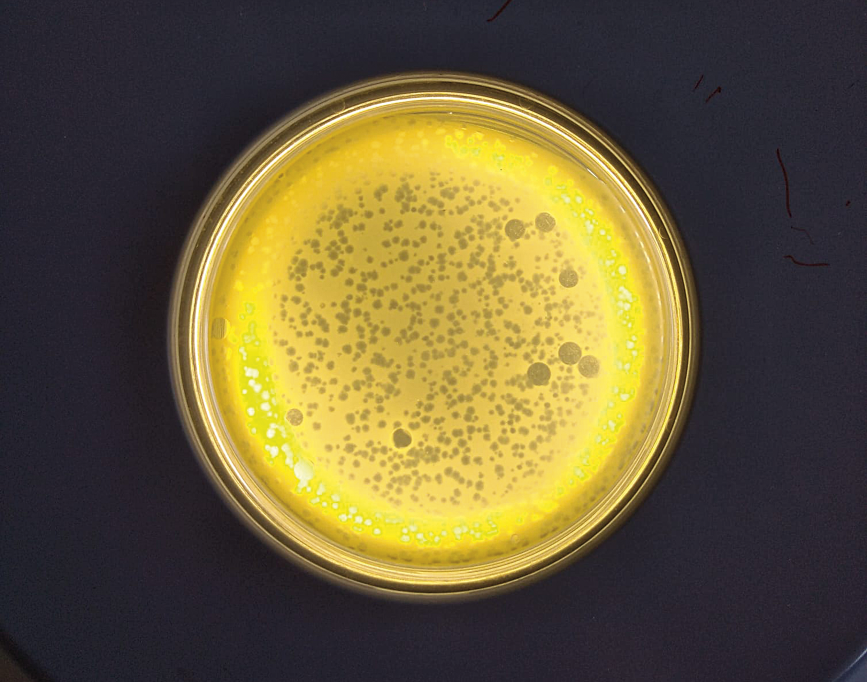
Figura 2. Figura 2. Ejemplo de placa de Petri con cultivos bacterianos en agar semisólido, donde se observa la presencia de halos o calvas de lisis, que reflejan la acción de los fagos lisando las bacterias que crecen en la placa. Hay dos fagos distintos, uno que produce calvas grandes y otro que las hace pequeñas. La lisis supone la ruptura de la membrana celular de la bacteria y la liberación del virus al medio extracelular. Imágenes tomadas en el Laboratorio de Virología Ambiental y Biomédica del Instituto de Biología Integrativa de Sistemas (UV-CSIC)./ Amanda Martínez
A día de hoy, los países occidentales carecen de legislación específica y de ensayos clínicos reconocidos y validados por las agencias regulatorias para el uso de fagos en pacientes. Este solo está permitido en casos excepcionales como tratamiento compasivo. Sin embargo, científicos y médicos de todo el mundo estamos solicitando a las agencias regulatorias la necesidad de incluir la terapia de fagos como tratamiento reconocido. En nuestro país, desde la Red Española de Bacteriófagos y Elementos Transductores (FAGOMA), estamos iniciando la tramitación a través de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) para facilitar su reconocimiento como tratamiento efectivo contra bacterias multirresistentes.
Los fagos en investigación básica
Los fagos han sido ampliamente utilizados para comprender procesos biológicos fundamentales como la replicación, la transcripción y la traducción de los ácidos nucleicos. Cabe destacar que una gran cantidad de productos derivados de fagos se utilizan habitualmente como reactivos en la investigación, como es el caso de las ligasas y las polimerasas. En España, la patente del método de amplificación de ácidos nucleicos basado en la ADN polimerasa obtenida a partir del fago phi29 –descubierta por Margarita Salas– continúa siendo la más rentable que ha presentado el CSIC. De hecho, esta tecnología es considerada uno de los grandes hitos de la historia de la ciencia en nuestro país. Asimismo, recientes premios Nobel de Química han sido atribuidos a investigaciones basadas en fagos. En 2018, Frances Arnold, George P. Smith y Gregory Winter fueron galardonados por desarrollar un método basado en fagos como vectores para la clonación o expresión de genes, conocido como phage display, que permite la evolución dirigida de enzimas y anticuerpos. Mediante esta técnica, pueden combinarse proteínas de interés en la parte externa de un fago para crear bibliotecas de proteínas que podrán ser útiles en diversos campos como el desarrollo de anticuerpos, el estudio de interacciones proteína-proteína, o la producción de antivirales o antitumorales, entre muchas otras aplicaciones. Recientemente, en 2020, Emmanuelle Charpentier y Jennifer Doudna fueron premiadas por la traslación del sistema inmunitario de las bacterias frente a los fagos a su uso como «tijeras genéticas», conocido como CRISPR-Cas9. Esta herramienta permite realizar cambios en el ADN de cualquier organismo con una elevada precisión. Estos son solo algunos ejemplos del uso de fagos como modelo experimental en ciencia básica y sus potenciales aplicaciones en la actualidad.
Los fagos en biomedicina
Los fagos se consideran herramientas muy prometedoras en el campo de la biomedicina por su utilidad en la prevención, diagnóstico y tratamiento de enfermedades bacterianas. Aunque su uso más conocido es la terapia de fagos, existen otras aplicaciones que suscitan gran interés como es el caso de los biosensores, las terapias antitumorales, las vacunas basadas en fagos o los vehículos dirigidos contra dianas específicas en el campo de la nanomedicina. Así, el potencial de los fagos como herramientas biomédicas es cada vez mayor, gracias a su fácil manipulación, alta especificidad y bajo coste de producción. Sin embargo, todavía existen puntos débiles, como la necesidad de revisar los aspectos éticos y los protocolos de regulación de su uso en biomedicina. Aquí vamos a detallar algunas de las aplicaciones de los fagos en biomedicina, con el objetivo de dar a conocer su potencial desde diferentes aproximaciones.
Los fagos en prevención
La piel, las superficies mucosas o el tracto digestivo son ejemplos de compartimentos en los que viven bacterias, virus y otros microorganismos que forman el microbioma. Fagos y bacterias coevolucionan constantemente y lo mantienen en equilibrio. En este sentido, los fagos pueden utilizarse como «probióticos» para controlar las comunidades bacterianas y prevenir enfermedades asociadas a un crecimiento bacteriano inadecuado. De nuevo, cabe destacar que los fagos son altamente específicos de las bacterias que son capaces de reconocer –gracias a receptores concretos que poseen–, y esta característica es clave para controlar cepas bacterianas de interés, puesto que las bacterias no diana permanecen inalteradas y mantienen la homeostasis (Figura 3). Los fagos, por tanto, pueden ser considerados moduladores de la microbiota y herramientas, ya que forman parte del entorno natural del microbioma.
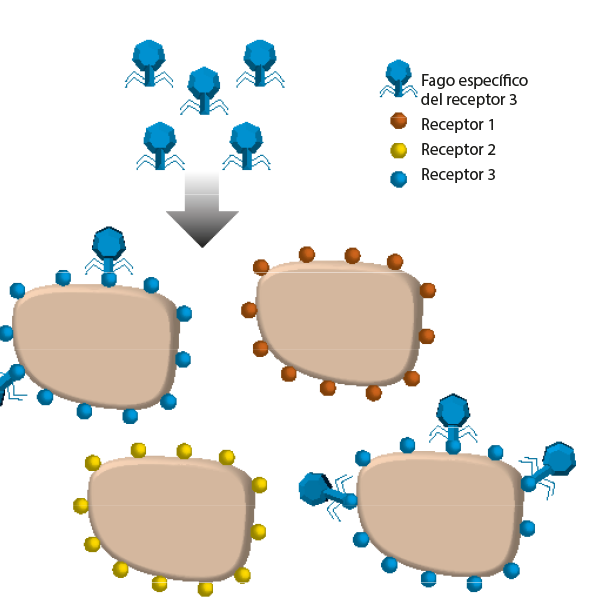
Figura 3. Debido a su alta especificidad, los fagos solo pueden reconocer las células que expresan receptores específicos. En la figura, podemos observar este proceso de reconocimiento y unión de un determinado fago a una bacteria diana. De esta manera, se previene la infección del resto de bacterias y posibles efectos secundarios en la microbiota./ Redibujado a partir de Pilar Domingo-Calap
Otro uso de los fagos en la prevención de enfermedades son las vacunas derivadas de fagos. La ingeniería de fagos basada en el phage display puede utilizarse para producir vacunas específicas contra otros patógenos como los hongos o incluso otros virus (Smith, 2019). Otra aplicación es generar bibliotecas de fagos para la producción de anticuerpos recombinantes. En este caso, los anticuerpos obtenidos pueden utilizarse como agentes profilácticos, pero también como herramientas de diagnóstico, de tipificación bacteriana o terapéuticas.
Los fagos también pueden combatir biopelículas bacterianas. En entornos hospitalarios, estas biopelículas se forman en dispositivos médicos, catéteres, prótesis, o incluso en superficies, y suelen estar compuestas por bacterias nosocomiales resistentes a antibióticos. Los fagos, gracias a su capacidad de replicación in situ y a enzimas codificadas en sus genomas, pueden destruir activamente estas biopelículas, ya que pueden penetrarlas y eliminarlas de forma muy eficiente. Por esta razón, los fagos podrían utilizarse para tratar dispositivos médicos o las superficies antes de su uso. Cabe destacar que algunas enzimas derivadas de fagos, como es el caso de las lisinas o las holinas, también tienen un gran potencial para combatir bacterias (Ferriol-González y Domingo-Calap, 2020).
Los fagos en diagnóstico
Como hemos mencionado, los fagos también pueden ser utilizados para la detección y tipificación de bacterias, una solución rápida y económica para una tarea que a veces resulta laboriosa y difícil. Si disponemos de una librería de fagos capaces de reconocer una batería de bacterias de interés, podemos determinar de forma sencilla qué bacteria está causando una infección. En este sentido, la bioimagen y la biodetección basada en fagos se considera de especial relevancia en biotecnología. Además, es posible vincular marcadores específicos en los genomas de los fagos para detectar mediante imágenes o sensores por dónde se extienden los fagos y hacer un marcaje in situ, lo que puede ayudar al diagnóstico de enfermedades bacterianas y a su localización concreta en el paciente, ya que los fagos son muy sensibles y pueden detectar bacterias en cantidades muy bajas (Van der Merwe et al., 2014).
Los fagos como tratamiento
El uso indiscriminado de antibióticos ha provocado la emergencia de bacterias multirresistentes o superbacterias. Por desgracia, a día de hoy existen cepas bacterianas que no pueden ser tratadas con ninguno de los antibióticos disponibles. Este problema se ha convertido en una amenaza mundial y requiere el desarrollo de tratamientos alternativos. De hecho, se prevé que en el año 2050 haya unos diez millones de muertes al año relacionadas con superbacterias resistentes, más muertes que por cáncer (Kraker et al., 2016).
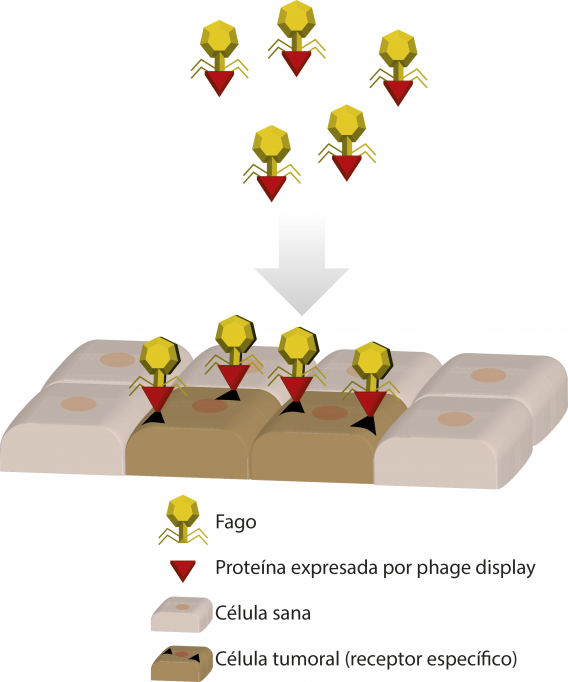
Figura 4. Fagos modificados genéticamente para expresar proteínas exógenas y poder reconocer células eucariotas de interés como, por ejemplo, células tumorales. Estas células expresan receptores específicos que pueden ser reconocidos gracias a las nuevas proteínas expresadas en los fagos mediante modificación genética o phage display. Una vez reconocida la célula tumoral, el fago puede actuar como vehículo de moléculas antitumorales o inducir la muerte celular./ Redibujado a partir de Pilar Domingo-Calap
En los últimos años, en Europa se están realizando los primeros ensayos clínicos en terapia de fagos, y recientemente, a causa de la pandemia ocasionada por el SARS-CoV-2, EE. UU. ha permitido el uso de fagos en pacientes de COVID-19 en cuidados intensivos. La razón principal es que la mitad de los fallecimientos en unidades de cuidados intensivos se debían a infecciones secundarias ocasionadas por superbacterias nosocomiales causantes de neumonías y sepsis. En concreto, Acinetobacter baumannii, Staphylococcus aureus y Pseudomonas aeruginosa han sido tratadas con éxito con fagos en este tipo de pacientes. Así, aunque la falta de legislación dificulta su uso en la práctica clínica, poco a poco va aumentando el número de personas tratadas con fagos. Más allá de la COVID-19, a fecha de hoy son los propios pacientes (en ocasiones, el personal médico) quienes se ponen directamente en contacto con investigadores expertos en fagos para intentar conseguir virus específicos capaces de controlar las infecciones bacterianas diana. De hecho, pacientes con infecciones provocadas por superbacterias sin tratamiento han realizado llamadas de socorro a través de redes sociales para encontrar fagos como alternativa terapéutica. Afortunadamente, algunos de ellos han sido tratados con éxito, lo que abre las puertas a la terapia de fagos como tratamiento contra bacterias patógenas (Kortright et al., 2019). Este proceso es todavía lento y complejo, pero cada vez hay más laboratorios implicados que estamos generando bibliotecas de fagos que permiten agilizarlo.
En contraste con el amplio espectro de acción de los antibióticos, como hemos comentado previamente, los fagos son altamente específicos, lo que resulta de especial interés para reducir efectos secundarios, ya que el microbioma permanecerá en equilibrio y solo se destruirán las bacterias diana. En el caso de la terapia con fagos, es importante utilizar fagos líticos capaces de lisar rápidamente las bacterias de forma eficiente. Cabe destacar que se ha propuesto también el uso de terapias combinadas de fagos con antibióticos, ya que se ha visto que podría haber un efecto sinérgico combinando ambos tratamientos.
Otra aplicación terapéutica de los fagos es, de nuevo, a través del phage display. Es posible modificar genéticamente los fagos para dirigirlos a células de interés, incluyendo células eucariotas. Así, los fagos pueden utilizarse como vehículos para entregar genes o fármacos en las células deseadas, técnica de especial interés en oncología, ya que se pueden diseñar fagos contra células tumorales (Figura 4).
Conclusiones
El uso de los fagos en biomedicina es muy amplio y permite abordar la problemática de las bacterias resistentes desde muchos puntos de vista (Domingo-Calap y Delgado-Martínez, 2018). Estas prometedoras herramientas presentan además ciertas ventajas frente a los antibióticos, como es su bajo coste de producción, que permitiría su uso en todo el mundo, incluyendo países poco desarrollados. Por otra parte, igual que han emergido resistencias a antibióticos, las bacterias pueden desarrollar resistencia a los fagos. Sin embargo, al contrario de los antibióticos, que son moléculas químicas estables, los fagos evolucionan y se adaptan, y pueden contrarrestar las resistencias. Además, es posible reducir la emergencia de resistencias mediante la evolución dirigida de los fagos en el laboratorio. Otra solución es el uso de cócteles de fagos, en los que se puede reducir la aparición de resistencias de forma significativa.
Sin embargo, a pesar de la gran versatilidad de los fagos y de resultados muy prometedores, todavía existen puntos débiles para su implementación en la práctica clínica. Los principales problemas son la falta de legislación y su aceptación por parte del público general. Los fagos son virus y su uso puede verse bloqueado por preocupaciones éticas. Por estas razones, se necesitan protocolos de regulación para dar seguridad y confianza a la población. Ensayos y pruebas clínicas siguiendo una normativa (todavía inexistente) son necesarios para demostrar la seguridad de los fagos en los seres humanos. En este sentido, es importante destacar que los fagos no son capaces de infectar células eucariotas (salvo que los modifiquemos genéticamente como hemos comentado), lo que hace que sean biológica y ecológicamente seguros. Cabe destacar también que las investigaciones realizadas hasta ahora no apuntan a un reconocimiento de los fagos por parte del sistema inmunitario, por lo que no habría respuesta específica contra los fagos, lo cual facilita su administración, incluyendo mediante vía intravenosa.
La enorme diversidad de fagos es también de especial interés a nivel ecológico, ya que se están descubriendo nuevas especies y observando una biodiversidad inexplorada hasta ahora, que puede llevar a nuevas aplicaciones. Además, nuevas tecnologías vinculadas a los fagos ayudarán a crear mejores herramientas en la práctica clínica. Un ejemplo interesante es la nanotecnología, que puede mejorar la estabilidad de los fagos, ayudar en su vehiculización o en la creación de biosensores. Las aproximaciones multidisciplinares en el campo de la biomedicina nos ayudan a explorar nuevas vías y a proponer nuevos tratamientos personalizados de rápida respuesta y menores efectos secundarios.
Para terminar, debe destacarse que el uso de fagos no está relegado a su uso en clínica, sino que puede tener aplicaciones en muchos otros campos como en la agricultura o la ganadería. Los mismos principios que hemos estado comentando se pueden aplicar a bacterias fitopatógenas o que causen enfermedades en animales. Este tipo de aproximaciones también se está empezando a implementar en la industria agroalimentaria, por ejemplo, en Estados Unidos y en algunos países de la Unión Europea, donde el uso de fagos está permitido para el control de bacterias patógenas tanto en cadena de producción de alimentos como en el producto final (Moye et al., 2018). Concretamente, existen preparados de fagos comerciales contra bacterias como Escherichia coli, Salmonella sp., y Listeria monocytogenes. Su comercialización como herramientas de biocontrol en seguridad alimentaria está dando muy buenos resultados, tanto en la desinfección de superficies industriales como en la descontaminación de alimentos.
Los fagos se postulan como herramientas muy prometedoras en la lucha contra bacterias resistentes y, por tanto, es necesario invertir en este campo de estudio para aportar nuevos datos que favorezcan su regulación y su uso rutinario. Realizar tareas de divulgación y concienciación ciudadana es también de gran importancia para poder llegar al público general, para dar a conocer nuevas terapias de control de bacterias patógenas y abordar la problemática con un tratamiento ecológicamente seguro y sostenible. Y es que no todos los virus son malos. Hay virus buenos que nos pueden ayudar a controlar lo que podría ser la siguiente pandemia: las superbacterias.
Referencias
Domingo-Calap, P., & Delgado-Martínez, J. (2018). Bacteriophages: Protagonists of a post-antibiotic era. Antibiotics, 7(3), 66. https://doi.org/10.3390/antibiotics7030066
Ferriol-González, C., & Domingo-Calap, P. (2020). Phages for biofilm removal. Antibiotics, 9(5), 268. https://doi.org/10.3390/antibiotics9050268K
Kortright, K. E., Chan, B. K., Koff, J. L., & Turner, P. E. (2019). Phage therapy: A renewed approach to combat antibiotic-resistant bacteria. Cell Host & Microbe, 25(2), 219–232. https://doi.org/10.1016/j.chom.2019.01.014
Kraker, M. E. A. de, Stewardson, A. J., & Harbarth, S. (2016). Will 10 million people die a year due to antimicrobial resistance by 2050? PLOS Medicine, 13(11), e1002184. https://doi.org/10.1371/journal.pmed.1002184
Moye, Z. D., Woolston, J., & Sulakvelidze, A. (2018). Bacteriophage applications for food production and processing. Viruses, 10(4), 205. https://doi.org/10.3390/v10040205
Smith, G. P. (2019). Phage display: Simple evolution in a petri dish (Nobel lecture). Angewandte Chemie International Edition, 58(41), 14428–14437. https://doi.org/10.1002/anie.201908308
Van der Merwe, R. G., van Helden, P. D., Warren, R. M., Sampson, S. L., & van Pittius, N. C. G. (2014). Phage-based detection of bacterial pathogens. Analyst, 139(11), 2617–2626. https://doi.org/10.1039/C4AN00208C





