Los seres humanos tenemos principalmente tres tipos de «armas» externas para controlar las enfermedades infecciosas: la higiene, la vacunación y los fármacos antimicrobianos (como, por ejemplo, los antibióticos). Y un arma propia: nuestro sistema inmunitario. Y todas son necesarias, porque las enfermedades infecciosas están muy extendidas entre los humanos. Aunque se pueden sufrir a cualquier edad, los grupos de mayor riesgo son los niños (porque es la primera vez que entran en contacto con los microorganismos patógenos), las mujeres embarazadas y la gente mayor.
El descubrimiento de los antibióticos y su aplicación en el tratamiento de las enfermedades infecciosas son dos de los hitos más importantes de la medicina durante el siglo xx. Los resultados casi «milagrosos» observados con la penicilina a partir de 1941 promovieron una investigación masiva para obtener más tipos de antibióticos con diferentes dianas de acción. Estos esfuerzos se tradujeron en un gran número de nuevos compuestos útiles para la medicina obtenidos durante las décadas posteriores a la utilización clínica de la penicilina. En las últimas décadas, la incidencia e impacto de las epidemias infecciosas de origen bacteriano se han reducido espectacularmente. En 2010, la tasa de mortalidad por las enfermedades infecciosas se redujo al 3 %. Y aunque los antibióticos se desarrollaron inicialmente para el tratamiento de enfermedades infecciosas en los humanos, los potentes y evidentes efectos conseguidos llevaron lógicamente a usarlos en animales (ganadería y animales de compañía) y en plantas (agricultura). En la actualidad, el 30 % de los antibióticos se usan en el tratamiento y profilaxis de las enfermedades infecciosas bacterianas en humanos, mientras que en agricultura y ganadería se utiliza el 70 % de la producción.
En los últimos ochenta años las relaciones entre bacterias y los humanos han cambiado enormemente. Cada vez que una persona es tratada con un antibiótico, la microbiota normal de esta persona «sufre» los mismos efectos que el patógeno objetivo del tratamiento. El tratamiento prolongado de antibióticos puede provocar una disbiosis de la microbiota comensal (es decir, cambios en la riqueza y abundancia de diferentes grupos de la microbiota bacteriana intestinal). Pero también somos testigos de otro cambio, el que se produce entre las propias bacterias. Casi tan pronto como se supo que los microorganismos podían ser eliminados por ciertos agentes, también se reconoció que algunos microbios podrían sobrevivir a las dosis normalmente letales de estos. Una bacteria puede adquirir mecanismos de resistencia diferentes y, por tanto, ser resistente a varios antibióticos. Este hecho puede limitar las alternativas de tratamiento para la infección con una bacteria multirresistente. Así pues, las enfermedades infecciosas causadas por bacterias resistentes a los antibióticos aumentan el riesgo de muerte del paciente, así como el riesgo de dispersión de este microorganismo en la comunidad y el ambiente, y también los costes asistenciales. Según la OMS, las enfermedades infecciosas por bacterias resistentes a los antibióticos podrían causar diez millones de muertes en 2050. Actualmente, según el CDC (Centro para el Control y Prevención de Enfermedades), más de 700.000 personas mueren en todo el mundo de infecciones por bacterias resistentes, con 25.000 muertos solo en la Unión Europea.
Las principales causas de la aparición y propagación de este fenómeno de resistencia son el uso indebido de los antibióticos, y la transmisión de bacterias resistentes entre los seres humanos, los animales y el medio ambiente. Mientras que el uso de los antibióticos ejerce una presión ecológica sobre las bacterias y contribuye a la selección de los microorganismos resistentes, las malas prácticas de prevención y control de las infecciones, igual que también las condiciones higiénico-sanitarias inadecuadas, favorecen la propagación de estas bacterias.
«Una bacteria puede adquirir mecanismos de resistencia diferentes y, por tanto, ser resistente a varios antibióticos»
Determinar los genes de resistencia (el llamado resistoma), y su difusión en el ambiente, es una prioridad de salud pública, para identificar los microorganismos que puedan plantear riesgos para la salud humana. En el pasado, la propagación de las resistencias se pensaba que estaba «compartimentada», bien dentro de una comunidad (por ejemplo, de persona a persona, o de animal/alimento a persona) o bien dentro de los hospitales. En estas compartimentaciones, las rutas de dispersión típicas son a través del contacto directo persona-persona o transmisión indirecta, por aerosoles o alimentos contaminados en algún punto de su elaboración desde la granja al tenedor (por ejemplo, durante la producción animal, en el matadero, distribución a la industria, preparación por parte de personas que llevan el patógeno…). Las aguas residuales, las plantas de tratamiento de estas, los ríos, los aerosoles transmitidos por el aire, el polvo, el comercio de alimentos colonizados por bacterias (véase Mètode n.º 72, «Brotes de brotes bordes») y los desplazamientos mundiales han permitido la globalización de la resistencia a los antibióticos.
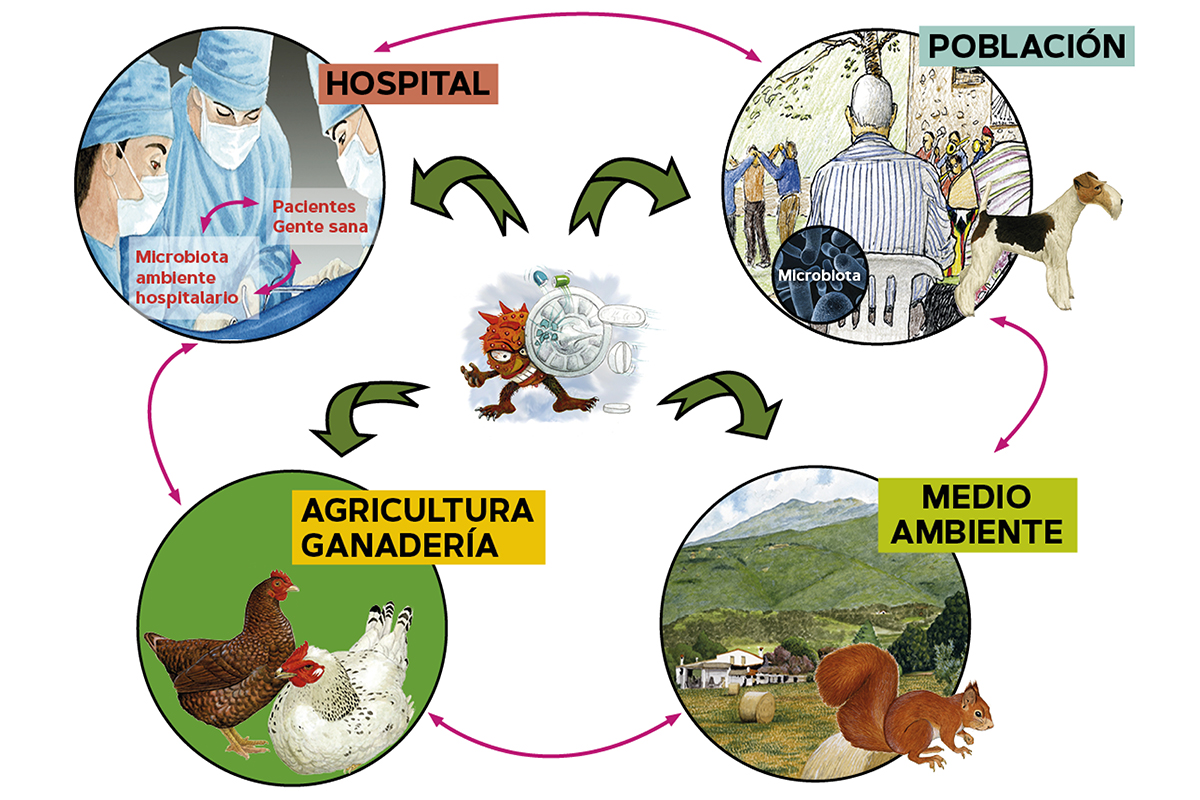
La resistencia a los antibióticos es un problema para la salud humana y, en consecuencia, su estudio tradicionalmente se ha enfocado hacia su impacto en el éxito del tratamiento de infecciones humanas en pacientes individuales (salud individual). Sin embargo, las bacterias resistentes a los antibióticos y los genes de resistencia a los antibióticos no se limitan solo a los pacientes infectados. La resistencia a los antimicrobianos es un problema ecológico que se caracteriza por interacciones complejas que implican varias poblaciones microbianas que afectan a la salud de los humanos, de los animales y del medio ambiente. El concepto actual de one health se define así: «El esfuerzo en colaboración de múltiples profesionales de las ciencias de la salud y de la vida, junto con las instituciones relacionadas (que trabajan a escala local, nacional y mundial) para conseguir una salud óptima para las personas, los animales domésticos y de vida salvaje, las plantas y nuestro entorno». Este intento de reducir o parar el adelanto de las resistencias a los antibióticos se basa en cuatro acciones: 1) mejorar la conciencia y la comprensión de la resistencia antimicrobiana con una eficaz comunicación, educación y formación; 2) fortalecer el conocimiento y la evidencia del problema de la resistencia a los antibióticos, a través de la vigilancia y la investigación; 3) reducir la incidencia de las infecciones mediante un saneamiento eficaz, higiene, y medidas de prevención de infecciones como las vacunas, y 4) optimizar el uso de medicamentos antimicrobianos en la salud humana y animal. Las acciones realizadas (o no realizadas) para contener la resistencia a los antimicrobianos en un «compartimento» (agricultura-ganadería, hospital, comunidad o ambiente) afectan a los otros compartimentos.
Que los antibióticos continúen siendo «balas mágicas» en el tratamiento de las enfermedades infecciosas empieza con la base de las acciones tomadas de forma individual, que se reflejarán en términos de comunidad y global. Cada uno de nosotros puede aportar su granito de arena para combatir esta pandemia silenciosa.