El reto de la investigación clínica
Decisiones terapéuticas basadas en la evidencia
El mejor instrumento que tenemos para tomar buenas decisiones clínicas es el método científico, en tanto que mecanismo libre, crítico y dinámico para poner a prueba las hipótesis correspondientes. El rasero del método científico se puede y se tiene que aplicar a todos los tratamientos y terapias con la necesaria flexibilidad pero al mismo tiempo con el mismo rigor, independientemente de su naturaleza, características o eventual y a menudo arbitraria clasificación como convencionales, complementarios o alternativos.
El reto de discriminar los tratamientos beneficiosos de los que no lo son
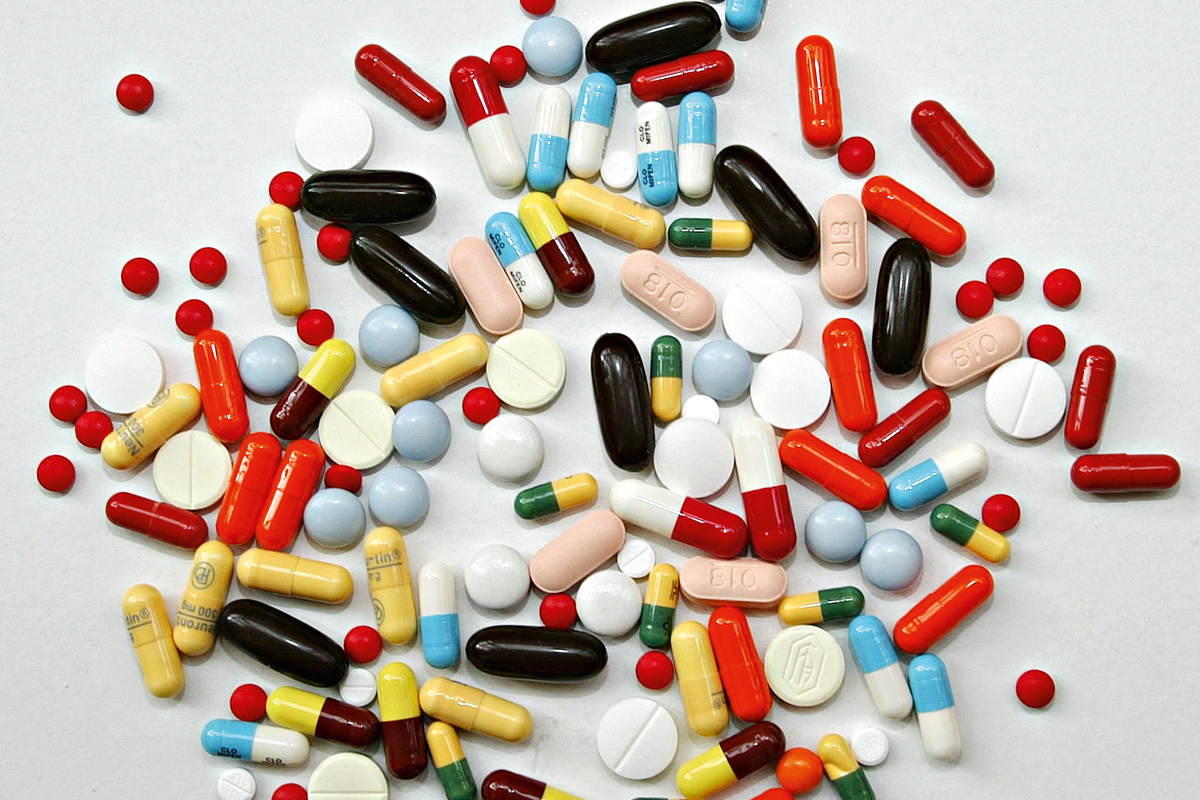
Hay que determinar hasta qué punto los beneficios atribuibles a los tratamientos son lo bastante fiables o no, especialmente cuando son tratamientos vitales, invasivos, agresivos o muy caros. Aunque los pacientes no sufran efectos adversos por recibir tratamientos poco eficaces, usarlos puede representar un derroche de recursos individuales y colectivos. Hace pocos años la publicación Clinical Evidence analizó la eficacia de 3.000 tratamientos. Un 11 % de estos estudios mostraba que los tratamientos eran beneficiosos; un 24 %, que probablemente lo eran, pero el resto tenían una eficacia desconocida, improbable o baja.
Una variabilidad extrema
Existe una amplísima variabilidad en el uso de determinados tratamientos. Las causas pueden ser múltiples, pero entre ellas tiene un lugar destacado la equívoca y contradictoria interpretación que se hace de la evidencia disponible, la cual muchas veces es realmente insuficiente, mientras que en otras ocasiones no se conoce, no se interpreta bien o se aplica mal. Por ejemplo, un trabajo reciente de nuestro grupo (Quintana, 2016) con datos de todos los hospitales españoles ha puesto en evidencia que el uso de la cirugía endovascular para tratar una afección tan grave como el aneurisma de aorta abdominal oscila entre el 3 % y el 78 %.
«Algunos médicos y pacientes tienden a atribuir al tratamiento utilizado las mejoras observadas, aunque no hayan tenido nada que ver»
La importancia del efecto placebo
Muchas enfermedades tienden a empeorar sin tratamiento y algunas empeoran a pesar de los tratamientos. No obstante, algunos problemas de salud mejoran por sí solos, es decir, son autolimitados porque la naturaleza humana la mayoría de las veces resiste y cura por sí sola. Pero por supuesto el tratamiento también puede empeorar las cosas. Algunos médicos y sobre todo los pacientes tienden a atribuir al tratamiento utilizado las mejoras observadas, aunque no haya tenido nada que ver. Por tanto, la investigación tiene que poder discriminar los verdaderos efectos de los tratamientos de aquellos atribuibles a la propia naturaleza o al efecto placebo (aquel efecto psicológico producido por una sustancia inerte). Recientemente hemos podido demostrar en un estudio controlado (De la Poza et al., 2016) que la no administración inmediata de antibióticos para tratar infecciones respiratorias leves es mejor que la prescripción sistemática de aquellos medicamentos, a los que a menudo se da el crédito de haber sanado afecciones autolimitadas.
Además, la inercia creada a lo largo del tiempo en muchos centros asistenciales no induce a plantearse críticamente si existen mejores alternativas terapéuticas que las que se están empleando. La propia experiencia clínica individual no debería ser enemiga de la evidencia generada mediante estudios clínicos hechos en otros pacientes.
«En nuestra sociedad predomina una cultura basada en el pensamiento optimista y consumista, y la atención sanitaria no es ninguna excepción»
Lo que es nuevo no siempre es mejor
En nuestra sociedad predomina una cultura basada en el pensamiento optimista y consumista, y la atención sanitaria no es ninguna excepción. Por ello, las novedades se presentan siempre como mejores, frecuentemente exagerando los efectos beneficiosos de los tratamientos, mientras que se quita importancia a los que son perjudiciales. La medicina acumula un bagaje de grandes y pequeños desastres de salud debidos a la introducción prematura y apresurada de nuevos tratamientos sin que hubiesen sido evaluados suficientemente. El caso de la talidomida, que provocó malformaciones congénitas muy graves a los hijos de las embarazadas tratadas, o el de la epidemia de ceguera entre los recién nacidos prematuros expuestos a altas concentraciones de oxígeno son emblemáticos de esa historia dolorosa.
Más no quiere decir necesariamente más beneficioso
La búsqueda de la intensidad correcta, la que ofrezca amplios beneficios y cause pocos efectos adversos, es un reto común para todos los tratamientos, pero este tipo de estudios no son habituales y las decisiones correspondientes se acaban tomando de manera subjetiva. A menudo, a medida que la dosis o la duración se incrementa, los efectos beneficiosos llegan a un techo pero generalmente los efectos adversos aumentan. La aspirina es un buen ejemplo de ello: a dosis bajas ayuda a prevenir los accidentes cerebrovasculares y tiene muy pocos efectos adversos, mientras que las dosis más elevadas aumentan el riesgo de hemorragia.
Anticiparse no siempre es bueno
La prevención secundaria o igualmente llamada detección precoz tiene como objetivo identificar lesiones o marcadores con riesgo de tener una enfermedad importante mediante una prueba de cribado. Por fuerza nos tenemos que preguntar si los beneficios de realizar una determinada prueba de cribado realmente superan los riesgos y los inconvenientes, que también los hay. El contraste entre el gran incremento de casos de cáncer de próstata detectados a partir de la determinación masiva del antígeno prostático específico y la no reducción de la mortalidad por esta enfermedad es un ejemplo muy ilustrativo.
El papel de la industria
Para llevar a cabo los correspondientes estudios clínicos y al mismo tiempo tener una mayor credibilidad, las compañías propietarias de los productos necesitan de investigadores que recluten a los pacientes pertinentes y que después divulguen sus resultados. Si serán más o menos fiables estos resultados dependerá de la influencia que hayan tenido los conflictos de interés, llamados así porque pueden entrar en contradicción los intereses de los pacientes, a los que los médicos y médicas están comprometidos deontológicamente a respetar, y los intereses de las empresas financiadoras de la investigación y a menudo de los propios investigadores. Desentrañar estas relaciones entre la investigación y el negocio no es fácil, a pesar de la progresiva exigencia de hacer explícitos los conflictos de interés existentes en el momento de publicar los estudios de investigación. En consecuencia, los estudios independientes sin conflictos de interés continúan siendo imprescindibles para facilitar a los médicos el cumplimiento de su papel de «evaluadores imparciales de los productos biomédicos que proponen a sus pacientes» (Relman, 1991).
La influencia del azar
Se necesitan estudios que no solo estén pensados para reducir los sesgos sino que también tengan en cuenta la posible intervención del azar, el cual puede llegar a confundir la dirección y magnitud de los resultados cuando los efectos terapéuticos son pequeños. Si además estos se intentan evaluar mediante estudios de un tamaño reducido, entonces se hará imposible distinguir entre las diferencias realmente atribuibles a los tratamientos y aquellas producidas por casualidad.
La presión de los afectados
Cuando se ha instalado un determinado estado de opinión, no pocas veces inducido o manipulado, de que algún tratamiento es eficaz, se hace difícil defender la necesidad de un estudio que compare ese tratamiento con uno convencional o con un placebo, ya que se presenta la propuesta como un intento de denegar el acceso a una terapia eficaz por razones de ahorro. En algunas enfermedades graves, los pacientes no han aceptado participar en los correspondientes estudios porque simplemente reclamaban que se administrase el tratamiento potencialmente milagroso de forma inmediata. En el caso de muchas terapias complementarias, como por ejemplo la homeopatía, los usuarios están tan convencidos de su eficacia que difícilmente aceptarían participar en una evaluación independiente.
«En muchos casos la industria es una parte muy influyente en las decisiones sobre qué temas se investigarán»
La no priorización de la investigación
Las preguntas clínicas de investigación deberían surgir de las incertidumbres y, limitaciones detectadas en la propia práctica clínica, a ser posible con la participación directa de los pacientes. Pero en muchos casos la industria es una parte muy influyente en las decisiones sobre qué temas se investigarán. Como consecuencia, se impulsan muchos estudios de investigación que tienen baja prioridad clínica; una buena parte de los nuevos tratamientos ofrecen pequeñas variaciones con respecto a los anteriores; difícilmente se investiga sobre intervenciones que no tienen valor comercial, como los consejos dietéticos, el ejercicio, la fisioterapia o el acompañamiento al final de la vida, por poner solo algunos ejemplos diversos.
La investigación redundante o innecesaria
Una buena parte de los estudios clínicos terapéuticos son redundantes y por tanto, innecesarios, independientemente del hecho de que sean buenos o malos. Se trata de trabajos que no aportan prácticamente nada nuevo en el mejor de los casos y que, en el peor, crean confusión y distorsiones entre sus destinatarios. Una de las principales faltas de estos estudios es que se diseñan sin haber consultado e integrado toda la evidencia previa existente sobre el tema, de forma que a menudo se repiten los errores o las limitaciones ya señaladas por anteriores autores.
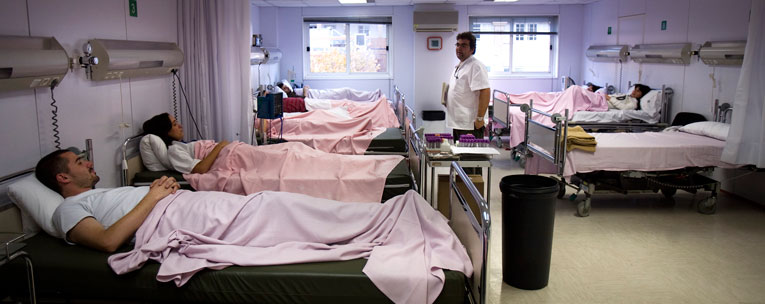
El mejor diseño de un ensayo clínico controlado es el de distribución aleatoria, un sistema que bien utilizado crea grupos de individuos perfectamente comparables. De esta forma, se pueden atribuir las posibles diferencias observadas a los diferentes tratamientos recibidos para cada uno. / Edu Bayer/SINC
Las comparaciones, la clave de los estudios terapéuticos
La necesidad de comparar grupos de pacientes que reciben tratamientos diferentes está planteada en la medicina desde hace mucho tiempo. Sin embargo, la única diferencia sistemática entre los grupos de pacientes debería ser los respectivos tratamientos que reciben, para poder atribuirles razonablemente las posibles diferencias observadas en los efectos y evitar que sean determinadas por el desigual pronóstico de los individuos incluidos en los grupos comparados. Las comparaciones que utilizan controles históricos son potencialmente problemáticas, porque siempre podemos dudar de si los grupos de comparación son similares o no. Sin embargo, si los controles son coetáneos y no históricos el reto continúa consistiendo en saber si los grupos de pacientes que reciben las diferentes intervenciones son lo bastante semejantes antes de empezar el tratamiento. Por ello, los resultados de los estudios observacionales empleados para dirimir preguntas terapéuticas se tienen que recibir siempre con mucha prudencia.
Un ejemplo claro de esta situación es la terapia hormonal sustitutiva, administrada durante muchos años para prevenir la enfermedad cardiovascular de acuerdo con estudios observacionales, y después abandonada cuando los ensayos clínicos llevados a cabo detectaron que los potenciales efectos adversos eran graves.
Para conseguir una asignación neutra e imparcial de los individuos a los diferentes tratamientos, el mejor diseño es el del ensayo clínico controlado con distribución aleatoria. Cuando el sistema de aleatorización está bien empleado, nos crea unos grupos de individuos perfectamente comparables. Entonces podremos atribuir razonablemente los resultados observados a los diferentes tratamientos recibidos por el grupo de intervención y el que actúa como control.
«Los ensayos presentan una serie de problemas metodológicos y logísticos que pueden llegar a aniquilar completamente su relevancia y credibilidad»
Sin embargo, los ensayos presentan también una serie de potenciales problemas metodológicos y logísticos que por su importancia pueden llegar a aniquilar completamente su relevancia y credibilidad: criterios demasiado restrictivos de selección, asignación o enmascaradamente incorrectos, desviaciones con respecto al protocolo inicial, tamaño insuficiente del estudio, interrupción prematura de los estudios, selección o análisis interesado de los resultados, abuso de las variables compuestas, poca consideración de los efectos adversos y burocratización excesiva de los procedimientos, por citar algunos de los más destacados.
Las revisiones sistemáticas, al rescate
Muchos de los problemas de los estudios clínicos primarios, como los ensayos clínicos controlados, pueden ser resueltos o por lo menos controlados por una buena revisión de la literatura. En efecto, revisar la literatura médica que ha intentado responder una determinada pregunta terapéutica representa ir más allá de un solo estudio primario y localizar todos los trabajos convenientes que hayan abordado la misma cuestión. De esta manera, la evidencia aportada por un determinado estudio se sitúa en el contexto del conocimiento existente y, por tanto, una revisión hecha con exhaustividad y rigor contiene una perspectiva global y al mismo tiempo concreta que la hace imprescindible (Higgins y Green, 2011).
Una revisión tiene que ser sistemática para integrar toda la evidencia empírica que cumpla con unos criterios de elegibilidad previamente establecidos. Utiliza métodos rigurosos y explícitos con el objetivo de minimizar los sesgos y aportar así unos resultados más fiables a partir de los cuales se puedan extraer conclusiones y tomar decisiones.
La importancia y el prestigio creciente que han ido adquiriendo las revisiones sistemáticas en muy buena parte es debida al impulso que les ha dado la colaboración Cochrane (Bonfill, 2014). Se trata de una red independiente y de alcance mundial de profesionales de la salud y también de ciudadanos y pacientes que tienen como principal objetivo producir, actualizar y difundir revisiones sistemáticas de las intervenciones clínicas y sanitarias. Las revisiones Cochrane, por su superior calidad metodológica y amplia difusión, se han convertido en referentes en todo el mundo.
Sin embargo, las revisiones sistemáticas no son una panacea, porque encaran también una serie de retos y problemas que no son pequeños y que conviene poner de relieve, como son la investigación primaria de mala calidad, los sesgos en la publicación, los métodos de revisión inadecuados o la redundancia de una buena parte de las revisiones que se publican.
Perspectivas de futuro para la investigación clínica
La investigación clínica es fundamental para poder mejorar la salud de las personas mediante la generación de información útil sobre los posibles efectos beneficiosos o adversos de una terapia. / National Eye Institute – NIH (EEUU) /(EUA)
Todo lo que hemos visto hasta ahora nos conduce a la necesidad de promover los valores éticos en la investigación clínica terapéutica y establecer los mecanismos a todos los niveles para aplicarlos a la práctica. Es también necesario incorporar las mejoras conceptuales, metodológicas y logísticas para que la información derivada de la investigación clínica terapéutica sea más adecuada.
Desde el punto de vista metodológico, en las últimas décadas hemos ido aprendiendo las múltiples maneras mediante las que se puede minar la fiabilidad de los ensayos clínicos. Pero al mismo tiempo se han desarrollado numerosos y variados métodos para prevenir muchos de aquellos errores y trampas, tanto las conscientes como las inconscientes. Además, se tiene que poder combinar la estructura esencial de los ensayos clínicos con la potencialidad de los marcadores que la investigación básica aporta continuamente. Se trata de la innovación de los diseños llamados adaptativos, en los que los investigadores de un ensayo identifican los resultados de un grupo de pacientes a los que ya se ha aplicado un tratamiento para decidir cómo se tratan los futuros pacientes que sean incluidos en el ensayo.
«Se tiene que poder combinar la estructura esencial de los ensayos clínicos con la potencialidad de los marcadores que la investigación básica aporta continuamente»
También hay que aprovechar toda la potencialidad de los estudios observacionales sin distribución aleatoria, es decir, aquellos estudios que tienen un grupo control que no se ha creado empleando el azar. Los estudios observacionales no solo son útiles para detectar los efectos adversos de los tratamientos que aparecen a medio y largo plazo o para evaluar los resultados del tratamiento cuando se incorporan a un determinado ámbito local o territorial. También es posible y necesario emplearlos y hacerlo con rigor cuando no se puede o no es lo bastante conveniente desarrollar un ensayo clínico, por ejemplo en el caso de enfermedades poco frecuentes o cuando los efectos terapéuticos esperables son muy grandes.
Además de mejorar la investigación primaria, también hay otros retos específicos para las revisiones sistemáticas, entre otros: registrar de forma prospectiva los protocolos de revisión en plataformas de acceso abierto; desarrollar las herramientas de apoyo tecnológico para enlazar los estudios primarios con las revisiones sistemáticas y hacer más eficiente el proceso de revisión; asumir y estandarizar mejor la combinación de los resultados derivados de los ensayos clínicos con los de los estudios observacionales, tanto por lo que respecta a los efectos adversos y costes como en relación a la eficacia cuando eso sea conveniente.
«Los estudios empíricos sugieren que la mayoría de los efectos terapéuticos que se han encontrado en la investigación médica son falsos positivos»
No cabe duda de que la investigación clínica terapéutica es fundamental para poder mejorar la salud de las personas mediante la generación de información útil sobre sus posibles beneficios y efectos adversos. Sin embargo, los estudios empíricos sugieren que la mayoría de los efectos terapéuticos que se han encontrado en la investigación médica son falsos positivos o se han exagerado sustancialmente, de forma que un excesivo número de avances científicos prometedores no acaban cumpliendo ni mucho menos las expectativas. Necesitamos más recursos públicos para impulsar la investigación clínica independiente y de calidad pero al mismo tiempo hay que reducir al máximo aquella que tan solo aporta confusión y retraso en la aplicación de las decisiones clínicas bien fundamentadas.
Este artículo es un resumen del discurso de presentación de Xavier Bonfill Cosp como miembro numerario de la Sección de Ciencias Biológicas del Institut d’Estudis Catalans.
REFERENCIAS
Bonfill, X. (2014). La colaboración Cochrane cumple 20 años. Medicina Clínica, 143(5), 210–215. doi: 10.1016/j.medcli.2014.02.003
Chalmers, I., Bracken, M. B., Djulbegovic, B., Garattini, S., Grant, J., Gülmezoglu, A. M., … Oliver, S. (2014). How to increase value and reduce waste when research priorities are set. The Lancet, 383, 156–165. doi: 10.1016/S0140-6736(13)62229-1
Clinical Evidence. What conclusions has Clinical Evidence drawn about what works, what doesn’t based on randomised controlled trial evidence? Consultado el 26 de febrero de 2016 en: http://clinicalevidence.bmj.com/x/set/static/cms/efficacy-categorisations.html
De la Poza Abad, M., Mas Dalmau, G., Moreno Bakedano, M., González González, A. I., Canellas Criado, Y., Hernández Anadón, S., … Delayed Antibiotic Prescription (DAP) Group. (2016). Prescription strategies in acute uncomplicated respiratory infections: A randomized clinical trial. JAMA Internal Medicine, 176(1), 21–29. doi: 10.1001/jamainternmed.2015.7088
Higgins, J. P. T., & Green, S. (Eds.). (2011). Cochrane handbook for systematic reviews of interventions version 5.1.0 [updated March 2011]. The Cochrane Collaboration, 2011. Consultado en www.cochrane-handbook.org
Quintana, M. J. (2016). Estudio de la variabilidad y de la adecuación clínica del tratamiento quirúrgico del aneurisma de aorta abdominal (Tesis doctoral inédita). Universitat Autònoma de Barcelona, España.
Relman, A. S. (1991). The health care industry: Where is it taking us? The New England Journal Medicine, 325, 854–859. doi: 10.1056/NEJM199109193251205