Una caixa de sorpreses
El cerebro humano y la neurogénesis
La existencia de neurogénesis adulta en el cerebro de mamíferos, incluida nuestra especie, así como la identificación de las células responsables de dicha neurogénesis ha cambiado completamente la idea que teníamos de la organización de nuestro cerebro. El descubrimiento de la existencia de células madre en el cerebro adulto responsables de dicha neurogénesis abre nuevas perspectivas en el campo de la medicina regenerativa, por el potencial para restaurar áreas dañadas, pero para llegar a esto debemos ser capaces de establecer un preciso diálogo con ellas.
A pesar de los grandes esfuerzos de los investigadores por saber cómo funciona nuestro cerebro, todavía parece que estemos dando los primeros pasos. Este siglo empezó tras la denominada «década del cerebro», época que al finalizar nos dejó más preguntas que respuestas. Este hecho ha dado lugar a que muchos investigadores se planteen que, más que una década, lo que necesitamos es un «siglo del cerebro». A pesar de no estar definido como tal, puede que este sea ese siglo, ya que en estos últimos años se han realizado espectaculares avances que incluso han llegado a derribar algunos de los grandes pilares en los que se apoyaba la neurociencia. Tal vez una de las mayores sorpresas ha sido el descubrimiento de la existencia de células madre neurales en el cerebro adulto de todos los mamíferos, incluyendo nuestra especie. Estas células presentan una localización precisa y hoy en día somos capaces de extraerlas, cultivarlas, amplificar su número…, pero todavía nos falta uno de los grandes retos, establecer un preciso diálogo con ellas.
«La neurogénesis adulta podría constituir un mecanismo adaptativo que contribuiría a la generación de memorias temporales y espaciales»
En animales de experimentación ya se han iniciado estas «conversaciones» en las que, a través de la utilización de algunas moléculas o factores de diferenciación, estamos comenzando a condicionarlas y dirigirlas, para que den lugar a células que sean capaces de incorporarse a circuitos existentes que estén lesionados. Este es un importante avance, ya que en un futuro estas células podrían ser utilizadas en terapias contra enfermedades neurodegenerativas tales como el Alzheimer, el Parkinson u otras patologías. No obstante, tenemos que ser conscientes de que se necesita un gran esfuerzo investigador, ya que esta realidad todavía está lejos de alcanzarse en la especie humana. Por ello, tal vez antes de empezar a controlarlas, deberíamos preguntarnos qué función cumplen estas células madre en el cerebro adulto.
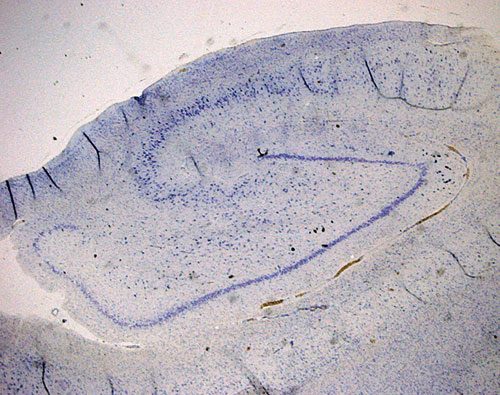
Fotografía panorámica del hipocampo humano. Las flechas señalan la banda celular del giro dentado donde se encuentran las células madre junto a las nuevas neuronas. La mayor parte de la neurogénesis adulta se produce en esta región./ Foto: © Jose Manuel García Verdugo y Arantxa Cebrián Silla
Células madre en cerebros adultos
Hoy en día sabemos que en el adulto estas células madre, lejos de estar en reposo, están activas y cumplen un papel: la generación de nuevas neuronas o neurogénesis. En nuestra especie, la mayor parte de la neurogénesis adulta se encuentra en el hipocampo, una región localizada en la región medial del lóbulo temporal y que está estrechamente relacionada con los procesos de aprendizaje y memoria. Dentro de la formación hipocampal, las células madre están ubicadas en una estructura particular que recibe el nombre de giro dentado. Estas células madre han sido descritas como células de tipo astroglial (células implicadas en el cuidado y soporte del sistema nervioso central).
Las células madre del giro dentado son las responsables de dar lugar a un tipo de neuronas denominadas neuronas granulares. Estas nuevas neuronas se integran en los circuitos hipocampales ya existentes y, a pesar de que conocemos su mecanismo de integración, todavía tenemos muchas preguntas acerca de qué función desempeñan estas nuevas neuronas en el cerebro humano. Sin embargo, la realización de estudios en roedores y la aplicación de modelos matemáticos ha permitido apuntar que esta neurogénesis adulta podría constituir un mecanismo adaptativo que contribuiría a la generación de memorias temporales y espaciales. Es decir, que la integración de nuevas neuronas en los circuitos establecidos facilitaría la discriminación entre contextos temporales o espaciales similares. Por lo tanto, este fenómeno podría estar favoreciendo la adaptación a situaciones cambiantes como podrían ser cambios estacionales, cambios ambientales o incluso la exposición a situaciones adversas tales como el estrés.
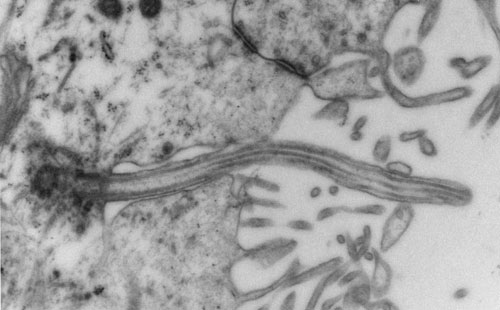
Cilio primario (señalado con flechas) visto al microscopio electrónico de transmisión y correspondiente a una célula madre de los ventrículos (V) laterales de un roedor. Esta estructura tubular concentra en su superficie receptores relacionados con el ciclo proliferativo. La alteración morfológica o la modificación de esta estructura bloquea la neurogénesis./ Foto: © Jose Manuel García Verdugo y Arantxa Cebrián Silla
Globalmente sabemos que el hipocampo no es una estructura aislada, sino que se encuentra ampliamente interconectada con diversas regiones, siendo la más importante la corteza cerebral. Estas conexiones son extremadamente complejas, ya que pueden ser tanto de naturaleza activadora como inhibitoria, así como altamente plásticas, es decir, que pueden modificarse de forma continua. La irrupción de la neurogénesis en el hipocampo ha obligado a ampliar este concepto de plasticidad y ha añadido un nuevo grado de complejidad a estas conexiones. De este modo, si imaginamos que el cerebro es un ordenador el giro dentado, con sus neuronas granulares, sería como un microchip en el que se comenzarían a formar los «circuitos electrónicos» de la memoria, funcionando como la base o portal de entrada de nueva información. Estos nuevos circuitos transmiten la información entrante a otras regiones del hipocampo y estas a su vez, al «disco duro» de nuestro cerebro, la corteza, donde se procesa y almacena la información. Una vez aquí, la nueva información podrá relacionarse con otras informaciones previamente almacenadas o incluso guardarse de forma independiente, al igual que introducimos en nuestros ordenadores nuevos archivos en carpetas previamente o nuevamente creadas.
«La mayor parte de la neurogénesis adulta se encuentra en el hipocampo, una región localizada en la región medial del lóbulo temporal y que está estrechamente relacionada con los procesos de aprendizaje y memoria»
La otra región cerebral donde se han identificado células madre está localizada en las paredes de los ventrículos laterales. Al igual que en el giro dentado, la naturaleza de estas células corresponde al tipo astroglial. En roedores, dan lugar a nuevas neuronas que migran varios milímetros (50 micras por hora) hasta alcanzar el bulbo olfatorio. Esta migración presenta una organización característica en la que las células migran, formando cadenas, por el interior de tubos celulares que les sirven de guía y aislamiento del resto del entramado nervioso. Al llegar al bulbo olfatorio, las células migradoras salen de estos tubos, migran radialmente y se integran como neuronas inmaduras en los circuitos preestablecidos y posteriormente se diferencian en neuronas de tipo granular y periglomerular. En roedores, este proceso tiene lugar a lo largo de toda la vida del animal y algunos estudios han puesto de manifiesto que la neurogénesis adulta en el bulbo olfatorio tiene un importante papel en el establecimiento de memorias olfativas.
Otro interesante avance realizado recientemente en el estudio de las células madre ha consistido en la interpretación de la función de una estructura conocida como cilio primario y que se caracteriza por ser una larga estructura tubular. Este cilio concentra en su superficie receptores relacionados con el ciclo proliferativo que funcionan a modo de antena receptora, y se ha visto que su alteración morfológica o la modificación de sus receptores bloquea la neurogénesis. Este descubrimiento ha sido aplicado al campo de la oncología, ya que se ha observado que las células madre tumorales también presentan un cilio primario.
«Una de las últimas sorpresas con la que nos hemos encontrado en el cerebro humano es una masiva migración neuronal que tiene lugar en las etapas más tempranas tras el nacimiento y que involucra de lleno a la corteza prefrontral»
Sorpresas en el cerebro humano
En el caso de la especie humana, la migración al bulbo olfatorio en etapas adultas es prácticamente indetectable, ya que, aunque algunos autores piensan que existe una migración celular individualizada, no se han encontrado cadenas o tubos celulares semejantes a los descritos en roedores. A pesar de no existir una migración de nuevas células al bulbo olfatorio humano adulto, existen evidencias de que hay células madre que persisten en las paredes de los ventrículos laterales. En algunas enfermedades o trastornos, tales como la esclerosis lateral amiotrófica (ELA) o el infarto cerebral, las células madre presentes en los ventrículos se activan y proliferan, dando lugar a nuevas células que migran a la zona de la lesión. Desconocemos el grado de incorporación de estas nuevas células y si su papel es relevante frente a patologías. Si en condiciones no patológicas nuestras células madre de los ventrículos laterales proliferan pero no hay migración al bulbo olfatorio, entonces ¿cuál es la función de dicha proliferación? La respuesta puede estar en que la mayoría de las veces centramos nuestra atención en la producción de neuronas, y las células madre también dan lugar a otro tipo celular como son los oligodendrocitos. Estas son las células responsables de formar la mielina a lo largo de los axones, protegiéndolos y dándoles soporte. Este es un campo todavía poco desarrollado y que necesita de investigaciones a largo plazo.
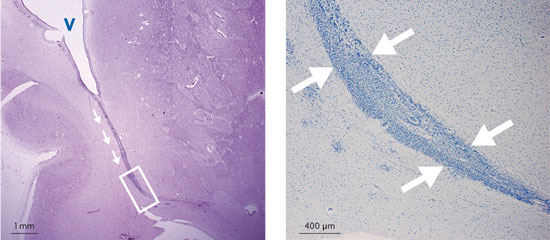
A la izquierda, fotografía panorámica del ventrículo (V) lateral de un cerebro humano de un mes de edad, donde se observa la gran cadena de células migradoras que se dirigen al bulbo olfatorio. A la derecha, detalle de este proceso. La investigación sobre este proceso está todavía poco estudiada y se necesita realizar estudios a largo plazo./ Foto: © Jose Manuel García Verdugo y Arantxa Cebrián Silla
Tal vez una de las últimas sorpresas con la que nos hemos encontrado en el cerebro humano es una masiva migración neuronal que tiene lugar en las etapas más tempranas tras el nacimiento y que involucra de lleno a la corteza prefrontal. Durante el desarrollo embrionario humano, se producen múltiples migraciones de nuevas neuronas hacia todas las regiones cerebrales, incluyendo los bulbos olfatorios. Tras el nacimiento y durante las primeras etapas lactantes (aproximadamente hasta los tres años de edad), la mayoría de las migraciones desaparece y permanecen las migraciones a los bulbos olfatorios, con una organización idéntica (migración en cadena a través de tubos celulares) a la observada en roedores y primates no humanos y que sería la responsable de la organización definitiva de los bulbos olfatorios. Lo sorprendente es que en el caso de los humanos la ruta de migración a los bulbos olfatorios se bifurca dando lugar a un nuevo pasillo de migración que termina en la corteza prefrontal.
Esta interesante migración de nuevas neuronas presenta las mismas características morfológicas que las previamente descritas en los bulbos olfatorios, aunque la escasez de este tipo de material todavía no ha permitido estudiar las diferencias que podrían existir a escala genética y molecular. Conocer los mecanismos celulares y moleculares por los que estas nuevas neuronas deciden separarse y tomar una ruta alternativa a la corriente hacia los bulbos olfatorios podría suponer un importantísimo paso para el conocimiento de la evolución del cerebro humano en comparación a roedores que no exhiben esta migración a la corteza prefrontal. Esta es una de las áreas más importantes de la corteza o «disco duro» humano. Se localiza en la parte más frontal de nuestro cerebro y está implicada en numerosas funciones cerebrales superiores, tales como la percepción, atención, memoria (memoria de trabajo o memoria operativa), lenguaje, toma de decisiones, etc. Estas funciones, junto con las de las áreas anatómicas del lenguaje, caracterizan el cerebro humano diferenciándolo del resto de mamíferos.
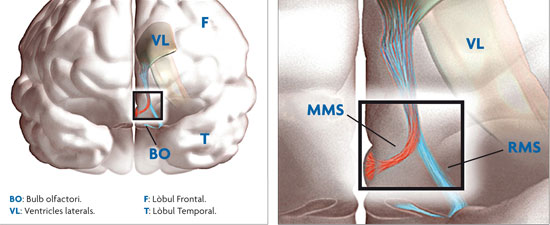
Esquema virtual 3D del cervell humà lactant, on es mostren les cadenes migradores que es dirigeixen cap al bulb olfactori (RMS) i cap a l’escorça prefrontal (MMS). Les cèl·lules migren formant cadenes per l’interior dels tubs cel·lulars fins arribar al bulb olfactori, on s’integren com a neurones immadures en els circuits preestablerts. Posteriorment, aquestes cèl·lules es diferencien en neurones de tipus granular i periglomerular. En cas del cervell humà, i a diferència del dels rosegadors, aquesta migració és pràcticament indetectable en l’etapa adulta./ Foto: © Jose Manuel García Verdugo i Arantxa Cebrián Silla
Aunque el campo de la neurogénesis adulta y la caracterización de las células madre para dialogar con ellas está creciendo de forma exponencial, no debemos olvidar a los investigadores que más han contribuido al conocimiento actual sobre el papel de la neurogénesis adulta. En primer lugar debemos citar a Joseph Altman, pionero en describir neurogénesis en el giro dentado y migraciones de nuevas neuronas hacia el bulbo olfatorio en roedores. Fernando Nottebohm, porque fue el primer investigador que relacionó la neurogénesis con la funcionalidad. Sus trabajos se realizaron en aves canoras, donde comprobó que las nuevas neuronas eran esenciales para que los canarios aprendieran nuevas canciones, lo que es fundamental para su reproducción. Lo más interesante es que cada año necesitan nuevas neuronas para aprender nuevas canciones y «borrar» las antiguas. Arturo Álvarez-Buylla, que junto a Joseph Altman y Giacomo Rizzolatti recibió el Príncipe de Asturias de Investigación en 2011, impulsó los estudios de neurogénesis adulta en mamíferos y describió por primera vez la naturaleza de las células madre en el giro dentado, y también de las células responsables de la neurogénesis hacia el bulbo olfatorio. Además fue el primero en identificar las células madre en el cerebro adulto humano.
«La existencia de neurogénesis adulta en el cerebro de mamíferos, incluida nuestra especie, así como la identificación de las células responsables de dicha neurogénesis, ha cambiado completamente la idea que teníamos de la organización de nuestro cerebro.»
La existencia de neurogénesis adulta en el cerebro de mamíferos, incluida nuestra especie, así como la identificación de las células responsables de dicha neurogénesis, ha cambiado completamente la idea que teníamos de la organización de nuestro cerebro. Si a esto le unimos que las tempranas migraciones neuronales podrían incrementar el volumen de la corteza prefrontal, y la incorporación de nuevas neuronas al hipocampo podría estar relacionada con procesos de memoria y aprendizaje, la idea que teníamos de nuestro cerebro ha dado un giro de 180 grados. Pero no debemos olvidar que, además, el descubrimiento de la existencia de células madre, su localización y naturaleza abre nuevas perspectivas en el campo de la medicina regenerativa, con el potencial para restaurar áreas dañadas, pero también plantea la necesidad de investigar la relación directa que hay entre células madre y tumores.
Deng, W. et al., 2010. «New Neurons and New Memories: How Does Adult Hippocampal Neurogenesis Affect Learning and Memory?» Nature Reviews Neuroscience, 11(5), 339-350.
Eriksson, P. S. et al., 1998. «Neurogenesis in the Adult Human Hippocampus». Nature Medicine, 4(11): 1313-1317.
Kempermann, G., 2012. «Youth Culture in the Adult Brain». Science, 335(6073): 1175-1176.
Sanai, N. et al., 2004. «Unique Astrocyte Ribbon in Adult Human Brain Contains Neural Stem Cells but Lacks Chain Migration». Nature, 427(6976):740-4.
Sanai, N. et al., 2011. «Corridors of Migrating Neurons in the Human Brain and Their Decline During Infancy». Nature, 478(7369): 382-386.





