Tras la pista del VIH
Los estudios y la comprensión del Sida

El VIH o virus de la inmunodeficiencia humana tiene un gran impacto sanitario, social y económico; las terapias actuales permiten controlar la infección pero no se ha encontrado tratamiento curativo ni vacuna efectiva. Para conseguir estos objetivos, debe tenerse en cuenta la gran variabilidad genética y rápida evolución del VIH, asociadas, por ejemplo, a la aparición de variantes de resistencia a fármacos o de cambios antigénicos.
Palabras clave: filogenia, biodiversidad, variabilidad genética, mutación, salud pública, virus.
¿Qué es el VIH i quina importancia té?
El sida o síndrome de la inmunodeficiencia humana adquirida es un problema de salud pública mundial: desde el descubrimiento del virus de la immunodeficiencia humana (VIH) en 1983 han muerto aproximadamente 30 millones de personas y hay más de 40 millones infectadas, la mayoría en países en vías de desarrollo. El VIH es un retrovirus que infecta específicamente células del sistema inmunitario que expresan el receptor de membrana CD4, principalmente los linfocitos T4. Como consecuencia, causa el debilitamientopaulatino del sistema inmunitario. En fases avanzadas, provoca la aparición de enfermedades oportunistas y algunos tipos de cáncer característicos del sida. En ausencia de tratamiento, la muerte se produce como media unos diez años tras la infección, aunque existe gran variabilidad en el tiempo de progresión de la enfermedad dependiendo de las características del virus y del sistema inmunitario del paciente.
«Mediante estudios evolutivos se puede tratar de predecir cómo responderá el virus a la presencia de fármacos, o qué variantes es más probable que se propaguen en un futuro»
El estudio de la evolución del VIH ha arrojado luz sobre su historia natural pero también sobre sus mecanismos de patogénesis. Mediante estudios evolutivos se puede además tratar de predecir, por ejemplo, cómo responderá el virus a la presencia de fármacos, o qué variantes es más probable que se propaguen en un futuro. De hecho, los estudios evolutivos han tenido un impacto positivo en el diseño del tratamiento de enfermedades humanas en general. Por ejemplo, la estimación de la tasa de mutación (probabilidad de aparición de cambios en el material hereditario) del VIH y del virus de la hepatitis C mostró que cada día aparecen en el interior de un paciente todos los cambios posibles de un solo nucleótido. Por tanto, la resistencia a fármacos es prácticamente inevitable a no ser que usen terapias combinadas que actúen sobre diferentes dianas y que requieran de la aparición de múltiples cambios genéticos en el virus para que éste desarrolle una resistencia.
Orígenes y epidemiología
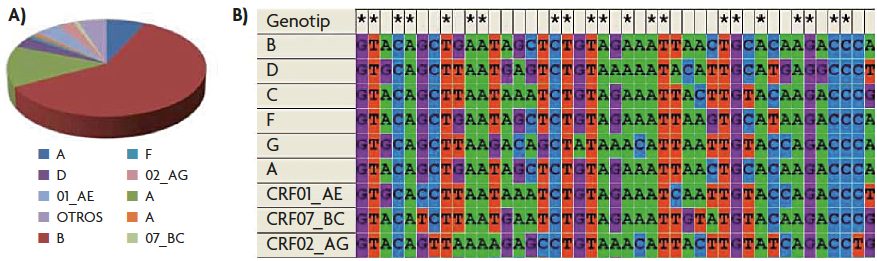
Los estudios de variabilidad y evolución nos han permitido saber que existen dos tipos de VIH, el VIH-1 y el VIH-2, con distinta procedencia geográfica y emparentados con distintos virus de la inmunodeficiencia de simios (VIS). Ambos se originaron como consecuencia de una zoonosis, es decir, una enfermedad que se transmite de animales a humanos. El VIH-1 se originó en los chimpancés tras uno o más eventos de recombinación entre distintos VIS que permitieron saltar la barrera de especie debido factores ecológicos o genéticos (Gao et al., 1999), mientras que el VIH-2 procede probablemente de VIS del mangabeye gris. El VIH-1 provoca la mayoría de las infecciones y es el más virulento de los dos tipos. La divergencia observada en el genoma completo el VIH-1 y el VIH-2 es aproximadamente del 40 % al 60 %. Entre distintos subtipos de VIH-1 puede llegar hasta el 35%, mientras que dentro del grupo M (que causa el 95 % de las infecciones por VIH) se ha estimado que está entre el 10% y el 30%. Los mayores valores de divergencia a se observan en el gen que codifica para la envuelta (env)(Brenner, 2007). En la figura 1 se puede observar la abundancia de los distintos genotipos de VIH-1 en el mundo y un ejemplo de la diversidad existente en el gen env entre los distintos genotipos de VIH-1.
«La transmisión del virus de madre a hijo prácticamente se puede eliminar si se aplica el tratamiento en las primeras semanas del embarazo»
La epidemiología se ocupa de estudiar la causa, incidencia, distribución y control de les enfermedades en las poblaciones humanas. Desde un punto de vista aplicado es importante unificar el proceso epidémico y la evolución de los patógenos, ya sea relacionado con la evolución de la resistencia a fármacos o de la virulencia del patógeno, el diseño de vacunas, o la emergencia de nuevos patógenos, y enfermedades transmitidas por estos. De especial interés es poder comprender cómo un patógeno puede invadir y propagarse exitosamente en la población. El informe de ONUSIDA de 2010 muestra que las nuevas infecciones por VIH están disminuyendo desde finales de los años noventa en la mayoría de países afectados en África subsahariana debido a medidas preventivas como el uso del preservativo. Contrariamente, en algunos países de Europa del Este y Asia central la incidencia del VIH ha aumentado. Además, el mayor acceso al tratamiento dio lugar a una disminución significativa de las muertes por VIH y la transmisión vertical o de madre a hijo puede ser casi prácticamente eliminada si se aplica el tratamiento en las primeras semanas del embarazo.
Mecanismos evolutivos
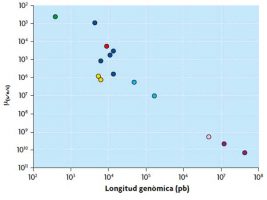
La mutación origina nueva variabilidad genética, mientras que la recombinación (en sentido amplio) produce gran variabilidad genética. Sobre esta variabilidad genética pueden actuar factores determinísticos (como la mutación, la migración o la selección) o aleatorios (deriva genética). Algunos virus usan el ARN como material genético en lugar del ADN, y estos se caracterizan por presentar tasas de mutación particularmente elevadas. Este es el caso del VIH, que usa para replicar su genoma una polimerasaespecial que copia ARN y lo convierte en ADN, llamada transcriptasa reversa. La mayoría de polimerasas que usan ARN como molde carecen de actividad correctora de errores y esto da lugar a mutaciones, lo que propicia que en una población viral exista variabilidad genética. En la fi gura 2 se puede observar cómo varía la tasa de mutación en distintos organismos. La mayor tasa de mutación se describió en un viroide de plantas; dentro del grupo de los virus, los de ARN poseen las mayores tasas de mutación, seguidos de los virus de ADN de cadena simple y virus de ADN de doble cadena; el VIH tiene una tasa de mutación que se encuentra dentro del rango de los virus de ARN. Los organismos con estructura celular poseen tasas de mutación unas 100.000 veces menores que las de los virus de ARN.
Otro aspecto muy importante en la evolución del VIH es la recombinación. El virión de VIH posee dos copias del genoma en forma de ARN y la transcriptasa reversa posee la capacidad de saltar de una cadena a otra durante la síntesis de ADN, lo que da lugar a moléculas recombinantes (Simon-Loriere y Holmes, 2011). La recombinación representó un papel clave en el origen del VIH y podría originar un nuevo tipo de VIH en el futuro. La recombinación puede tener efectos en la expansión del rango de hospedador, virulencia del virus, evasió del sistema immunitario del virus, evasión del sistema inmunitario o adquisición de resistencia a fármacos. Por ejemplo, la forma recombinante circulante 01_AE, una vez se estableció en el norte de Tailandia, aumentó su frecuencia y predominó rápidamente en el resto de Tailandia, Laos, Camboya y Vietnam (Stephens, 2005). La deriva genética es el proceso por el cual las frecuencias alélicas cambian al azar de una generación a la siguiente debido a efectos de muestreo en las poblaciones. Su intensidad es mayor cuanto menor es el tamaño poblacional, y en el caso del VIH ocurre principalmente en la transmisión entre personas, pues esta conlleva cuellos de botella en el tamaño de la población viral. De hecho está aceptado que la infección por VIH suele comenzar con la transmisión de una o pocas partículas infecciosas (Keele et al., 2008).
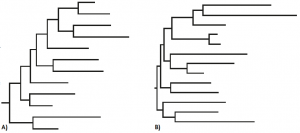
Los cuellos de botella también pueden ocurrir dentro del paciente, por ejemplo, en subdivisiones tisulares. La selección natural, a su vez, provoca cambios en las frecuencias alélicas actuando sobre mutaciones y/o genomas que influyen sobre la eficacia biológica. La selección puede ser adaptativa o positiva cuando se favorece la fijación de mutaciones que sean beneficiosas en determinado ambiente, o negativa cuando se eliminan mutaciones deletéreas. El sistema inmunitario del hospedador y los tratamientos con antivirales ejercen una fuerte presión de selección sobre el virus, como veremos a continuación. Los mecanismos evolutivos que actúan sobre las poblaciones viralespueden tener un papel diferente dentro del hospedador y entre hospedadores. Por ejemplo, cuando se observan las relaciones filogenéticas de variantes virales del gen env que codifica para la envuelta del virus podemos distinguir dos patrones distintos; por un lado las filogenias intrahospedador indican la acción de una presión de selección, mientras que los árboles filogenéticos interhospedador sugieren que la deriva tiene un papel más importante (Grenfell et al., 2004) (figura 3).
Escape del sistema immunitario
El sistema inmunitario del hospedador tiene un componente innato (inespecífico) y otro adaptativo (específico). La respuesta innata se caracteriza por la fiebre y la inflamación entre otros síntomas, los cuales están controlados por procesos como la secreción de citoquinas (por ejemplo, interferón). En el caso del VIH, además, la enzima (una proteína que edita ADN de cadena simple) participa en la respuesta innata y provoca mutaciones durante el proceso de síntesis del ADN viral del ARN que inactivan al virus. Para contrarrestar su efecto, el VIH incorporó a su genoma un gen denominado o factor de infectividad viral (vif) (Kirchhoff, 2010). En cuanto a la respuesta específica, en vertebrados existen una serie de genes que codifican para el complejo mayor de histocompatibilidad (MHC). Este presenta porciones de las proteínas virales denominadas epítopos, lo que permite la puesta en marcha de una respuesta immunitaria contra el virus.
«Una de les dificultades para el desarrollo de una vacuna contra el CIH-1 es la elevada variabilidad genética y la rápida genética y la rápida evolución del virus»
Las poblaciones humanas son extraordinariamente variables para los genes MHC y por tanto reconocen distintos epítopos virales. Se ha demostrado algunas variantes del MHC permiten responder mejor a la infección que otras y están asociadas a una progresión más lenta de la enfermedad (Buckheit III et al., 2012). Para entender esto, es necesario considerar la evolución del VIH dentro de los pacientes. La presión ejercida por la respuesta inmunitaria específica hace que se seleccionen mutantes del virus con capacidad para evadir esta respuesta. Sin embargo, estas mutaciones pueden comprometerla capacidad del virus para llevar a cabo su ciclo infeccioso si afectan a regiones importantes de las proteínas virales (regiones conservadas). Son precisamente aquellas variantes del MHC capaces de reconocer epítopos virales en regiones conservadas las que están asociadas a un mejor pronóstico.
Resistencia a los antivirales
Como los virus son parásitos intracelulares obligados y usan la maquinaria celular, es complicado encontrar compuestos que únicamente afecten a la actividad viral, ya que también pueden afectar negativamente a las células hospedadoras. Una aproximación al diseño de nuevos fármacos consiste, pues, en identifi car los pasos específi camente virales del ciclo infeccioso. La transcriptasa reversa y la proteasa encargada de procesar la poliproteína codifi cada por el VIH son dianas ideales, al ser exclusivas del virus. El primer compuesto contra la transcriptasa reversa que mostró efectividad fue la azotimidina (AZT), un análogo de nucleósido cuya estructura es similar a la de los nucleótidos que componen el ADN. Cuando en la célula está presente el AZT, la transcriptasa reversa lo añade por error a la cadena de ADN de nueva síntesis interrumpiendo la síntesis (fi gura 4). Sin embargo, se observó que tras uno o dos años de tratamiento, los pacientes con VIH dejaban de responder y la enfermedad seguía progresando. La resistencia se debía a mutaciones en el gen de la transcriptasa reversa, que eran convergentes, es decir, aparecían en poblaciones virales de diferentes pacientes.
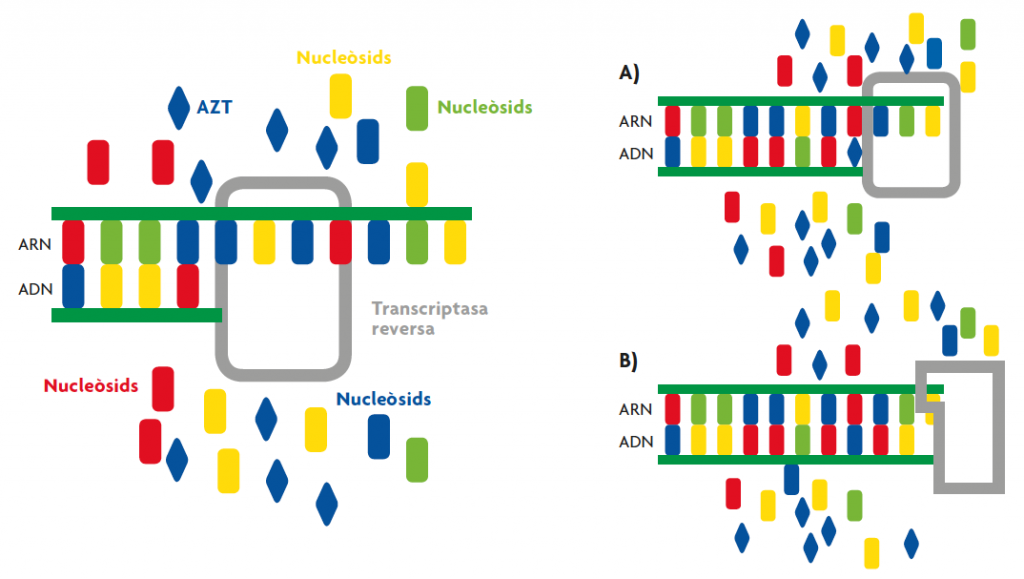
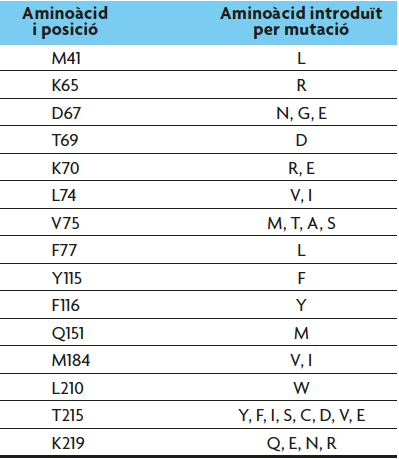
Algunas de las mutaciones descritas localizadas en el centro activo de la transcriptasa reversa son L74V y T215Y (la nomenclatura el cambio de aminoácido y la posición en la que ocurre) (Bennett et al., 2009) (tabla 1); además algunas causan resistencia cruzada a otros antivirales análogos de nucleósido (Margeridon-Thermet i Shafer, 2010). Debido a esto, la composición genética de la población de VIH cambió con el tiempo, en respuesta a la presencia del AZT. Esto es un claro ejemplo de evolución por selección natural. Consecuentmente el tratamiento actual consiste en combinaciones de tres o cuatro fármacos que incluyen inhibidores de la transcriptasa reversa y de la proteasa. Esta terapia combinada es muy efectiva bloqueando la replicación del virus y reduciendo la carga viral en la sangre. Sin embargo, como el virus está latente en algunas células, el bloqueo no es total, y eso permite que, potencialmente, puedan aparecer partículas virales resistentes, lo que impediría la erradicación del virus.
«La presión ejercida por la respuesta inmunitaria específica hace que se seleccionen mutanciones del virus con capacidad para evadir esta respuesta»
Diseño de vacunas
Una vacuna induce la respuesta inmunitaria específi a celular y humoral de modo que el individuo vacunado desarrolla una memoria inmunitaria que le permite combatir mejor al patógeno. Tradicionalmente se han usado distintas estrategias como los patógenos inactivados (por calor o químicamente), atenuados, o compuestos que los patógenos presentan en su superficie que actúan como determinante antigénico y son reconocidos por las células del sistema inmunitario. La vacunación ha tenido gran éxito en la prevención y control de varias enfermedades como la poliomielitis, la viruela, el sarampión, la rubeola o la gripe. En cambio, aún no se han desarrollado vacunas eficaces contra el VIH-1 o el virus de la hepatitis C. Una de las dificultades para el desarrollo de una vacuna contra el VIH-1 es la elevada variabilidad genética y la rápida evolución del virus. Al tener el VIH-1 una gran variabilidad, sobre todo en el gen que codifica para la proteína de la envuelta, una vacuna que proteja frente a un subtipo determinado podría no proteger o proteger parcialmente frente a otros subtipos del virus.
No obstante, los estudios epidemiológicos señalan que una vacuna con una baja eficacia podría disminuir la incidencia del VIH-1 en un porcentaje significativo (ONUSIDA, 2010). En esta línea, destaca el estudio llevado a cabo en el año 2009 en la población tailandesa. Los resultados de la fase III de ensayos clínicos mostraron una eficacia del 30 % en la protección contra el VIH. La vacuna consistía en la combinación de un vector que expresa inmunógenos (sustancias que inducen la respuesta inmunitaria adaptativa) del VIH-1 y una versión recombinante de la proteína de la envuelta (Rerks-Ngarm et al., 2009). Aunque este resultado no es suficiente para aplicar de forma generalizada la vacuna da pistas sobre hacia dónde deben orientarse nuevas investigaciones para mejorar la respuesta inmunitaria mediante nuevas construcciones, el uso de varias dosis o incluso la administración de más y/o mejores adyuvantes (potenciadores de la respuesta inmunitaria) que se suministren junto con esta.
Conclusiones y perspectivas de futuro perspectives de futur
Debido a la importancia del sida, se han destinado muchos recursos económicos para estudiar el VIH. Los principales objetivos de los grupos de investigación son desarrollar fármacos antivirales efcaces y una vacuna. Se ha cumplido en gran medida con el primer objetivo, sin embargo la obtención de una vacuna efi caz parece lejana. La alta variabilidad del VIH, debido a su elevada tasa de mutación y recombinación, junto con la latencia que caracteriza la infección, lo hace especialmente difícil de combatir. Por tanto, el conocimiento y la comprensión de los mecanismos evolutivos que gobiernan la evolución del VIH son clave para saber no solo cómo se originó la enfermedad, sino también cómo se desarrolla, cómo tratarla, cómo puede cambiar en el futuro e, idealmente, cómo erradicarla.
Referencias
Bennett, D. E. et al., 2009. «Drug Resistance Mutations for Surveillance of Transmitted HIV-1 Drug-Resistance: 2009 Update». PLOS One, 4: e4724. DOI: <10.1371/journal.pone.0004724>.
Brenner, B. G., 2007. «Resistance and Viral Subtypes: How Important Are the Differences and Why Do They Occur?». Current Opinion in HIV and AIDS, 2(2): 94-102. DOI: <10.1097/COH.0b013e32801682e2>.
Buckheit III, R. W. et al., 2013. «The Implications of Viral Reservoirs on the Elite Control of HIV-1 Infection». Cellular and Molecular Life Sciences, 70(6): 1009-1019. DOI <10.1007/s00018-012-1101-7>.
Gao, F. et al., 1999. «Origin of HIV-1 in the Chimpanzee Pan troglodytes troglodytes». Nature, 397: 436-441. DOI: <10.1038/17130>.
Grenfell, B. T. et al., 2004. «Unifying the Epidemiological and Evolutionary Dynamics of Pathogens». Science, 303(5656): 327-332. DOI: <10.1126/science.1090727>.
Keele, B. F. et al., 2008. «Identification and Characterization of Transmitted Early Founder Virus Envelopes in Primary HIV-1 Infection». PNAS, 105(21): 7552-7557. DOI: <10.1073/pnas.0802203105>.
Kirchhoff, F., 2010. «Immune Evasion and Counteraction of Restriction Factors by HIV-1 and Other Primate Lentiviruses». Cell Host and Microbe, 8(1): 55-67. DOI: <10.1016/j.chom.2010.06.004>.
Margeridon-Thermet, S. i R. W. Shafer, 2010. «Comparison of the Mechanisms of Drug Resistance Among HIV, Hepatitis B, and Hepatitis C». Viruses, 2(12): 2696-2739. DOI: <10.3390/v2122696>
ONUSIDA, 2010. Informe mundial. Informe del ONUSIDA sobre la epidemia mundial del SIDA. Disponible en: <http://www.unaids.org/en/media/unaids/contentassets/documents/unaidspublication/2010/JC1958_GlobalReport2010_full_es.pdf>.
Rerks-Ngarm, S. et al., 2009. «Vaccination with ALVAC and AIDSVAX to Prevent HIV-1 Infection in Thailand». The New England Journal of Medicine, 361: 2209-2220. DOI: <10.1056/NEJMoa0908492>.
Simon-Loriere, E. i E. C. Holmes, 2011. «Why do RNA Viruses Recombine?». Nature Reviews Microbiology, 9: 617-626. DOI: <10.1038/nrmicro2614>.
Stephens, H. A. F., 2005. «HIV-1 Diversity Versus HLA Class I Polymorphism». Trends in Immunology, 26(1): 41-47. DOI: <10.1016/j.it.2004.11.001>.





