Un ecosistema enfermo
La lucha contra la resistencia a antibióticos desde una perspectiva global

La producción antropogénica de antibióticos ha provocado una enfermedad de los ecosistemas microbianos de dimensión planetaria, cuya repercusión más inmediata para el hombre es la intratabilidad de las infecciones. La comprensión del fenómeno y las posibilidades de intervención requieren nuevos métodos conceptuales, analíticos y tecnológicos.
Palabras clave: estrategias eco-evo, medicina planetaria, resistencia a antibióticos, sistemas multijerárquicos.
Para prevenir y remediar la salud humana, la salud pública requiere información de carácter epidemiológico que describa la dimensión (incidencia y prevalencia) del fenómeno bajo estudio y permita inducir sus posibles asociaciones causales. Es cada vez más patente que la salud humana es dependiente de la salud global, esto es, de la salud de todo el medio ambiente en que el hombre está inserto. En este sentido, los esfuerzos para controlar las causas que pueden afectar negativamente a la salud humana deben abarcar el análisis de las enfermedades del hombre, pero también de todos los demás animales (one-health perspective), las enfermedades de los vegetales y de nuestra extensísima microbiosfera, el conjunto de microbios que cubren nuestro planeta sin conocer fronteras, y de cuya existencia y equilibrio depende la existencia de los seres que, sin mucha objetividad, llamamos superiores.
Una medicina planetaria
La salud humana depende de la que posea nuestro planeta. Por supuesto, el éxito biológico de Homo sapiens ha modificado profundamente la Tierra, de tal forma que se puede concebir que el hombre ha determinado una nueva época geológica, el Antropoceno, en la que la naturaleza ha quedado estresada y modificada por la acción del hombre. Esta actividad antropogénica determinará el futuro de la evolución biológica de nuestro planeta. El problema que aquí nos ocupa, el de la resistencia bacteriana a los antibióticos, es un buen ejemplo para ilustrar los efectos deletéreos para la especie humana de la modificación antropogénica del medio ambiente.
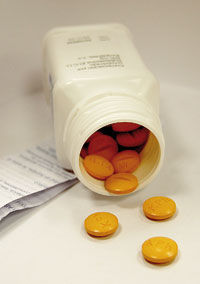
La producción industrial de los antibióticos ha creado una verdadera «polución antibiótica planetaria». Una de las enfermedades del planeta es debida a este efecto de la producción masiva de antibióticos que acaban liberándose al medio ambiente / Agencia SINC
Probablemente necesitaremos el establecimiento de una verdadera «medicina planetaria». La idea es que el planeta entero debe ser considerado como un «sujeto» que requiere atención médica. La refinada metodología médica destinada al enfermo individual debe escalarse a la dimensión del planeta, empezando por definir los signos y síntomas de las enfermedades planetarias, estudiando su patogénesis y patofisiología, tratando de evaluar las posibilidades de diseminación de la enfermedad al conjunto del planeta, estableciendo métodos para diagnosticarla, desde tecnologías de imagen a tecnologías avanzadas de identificación molecular, y con todo ello intentar realizar predicciones ecológicas y evolutivas. Esto se seguiría de la aplicación de intervenciones específicas, sin excluir la cirugía; desarrollo de tratamientos, como los futuros fármacos eco-evo1 (Baquero et al., 2011), métodos de contención y aislamiento, o incluso aplicación de cuidados intensivos y medidas preventivas. Como decíamos, el problema de la resistencia a los antibióticos es un problema-modelo para la futura medicina planetaria; sin duda el planeta está «enfermo de resistencia a los antibióticos», y esa enfermedad, que afecta a la microbiosfera, hace que muchos humanos estén colonizados por comunidades bacterianas anormales, frecuentemente microorganismos resistentes a los antibióticos.
El diagnóstico preciso de las enfermedades de la microbiosfera del planeta requiere mejorar la sensibilidad de nuestros criterios y métodos para medir la diversidad microbiana. Los cambios en la diversidad deben constituir uno de los análisis-clave para detectar los síntomas y evolución de la enfermedad. Sin duda este objetivo requiere en primer lugar una reconsideración de las unidades biológicas bacterianas. No podemos seguir utilizando la vieja clasificación linneana de las «especies microbianas». Por supuesto no podemos mantener seriamente que hay 20.000 especies bacterianas «bien definidas», si hemos identificado 300.000 especies de plantas o 10 millones de artrópodos. Debería haber al menos unos mil millones de especies bacterianas, según algunas estimaciones basadas en extrapolación matemática a partir de estudios metagenómicos. Por supuesto tenemos que mejorar nuestras técnicas de cultivo; la reciente propuesta de la «culturómica» (inóculo de muestras naturales en múltiples medios) probablemente mejorará nuestra capacidad analítica. Y, por supuesto, tenemos que redefinir el concepto de especie bacteriana.
La polución antibiótica
El hombre ha desarrollado la capacidad de producir substancias antimicrobianas para defenderse de las enfermedades infecciosas, que en forma individual o bajo el espanto de las grandes epidemias han asolado nuestra especie. Bajo el «paraguas protector» de los antibióticos se ha desarrollado toda la medicina moderna. Sin antibióticos una enorme proporción de nuestras personas mayores y nuestros recién nacidos (con defensas disminuidas ante la infección) morirían de infecciones. Sin antibióticos serían inconcebibles las unidades de cuidados intensivos, la terapia del cáncer, el cuidado de los niños prematuros, las cirugías complejas o los trasplantes de órganos. El problema es que la producción industrial de los antibióticos ha creado una verdadera «polución antibiótica planetaria». Una de las enfermedades del planeta es debida a este efecto de la producción masiva de antibióticos y la liberación en el medio ambiente.
La producción industrial de antibióticos es un ejemplo paradigmático del tipo de sustancias antropogénicas que ejercen un poderoso efecto en la microbiosfera. Con la producción anual de fármacos antibióticos se podría cubrir la superficie de la Tierra de una capa capaz de eliminar bacterias. No solo los antibióticos acaban inespecíficamente con trillones de bacterias, sino que esta eliminación va asociada a la selección de microorganismos resistentes. La importancia de la polución antibiótica del planeta no es tanto la selección de bacterias resistentes potencialmente patógenas para los humanos (y por tanto causantes de infecciones intratables), sino sobre todo los efectos de carácter «ecológico» que podrían resultar de la eliminación de poblaciones naturales y su substitución por otras. Incrementando las fuerzas selectivas y estimulando la capacidad de variación de los microorganismos (mutación, recombinación, transposición, modularización, transferencia genética) (Galán et al., 2013) los antibióticos de origen industrial están modificando la ecogenética de las bacterias y acelerando la evolución de la microbiosfera.
«El hombre ha determinado una nueva época geológica en la que la naturaleza ha quedado estresada y modificada por su acción»
Es esencial comprender que la mayor parte de los antibióticos son substancias naturales. En realidad, debe existir un número muy elevado (¿cientos de miles?) de antibióticos naturales, y solo una pequeñísima parte (menos de cien) han llegado a ser producidos industrialmente y utilizados en la medicina humana y animal. ¿Cuál es la función natural de los antibióticos? Los antibióticos son substancias que median en las comunicaciones intercelulares, substancias «organizadoras» de los ciclos vitales y la homeostasis de las poblaciones y comunidades microbianas. El papel de los antibióticos en la naturaleza no es necesariamente, como podría parecer a primera vista, el de intervenir como armas en la «guerra entre bacterias». Su efecto inhibidor del crecimiento de otros microorganismos tendría, en primer lugar, una función defensiva, no ofensiva; por otra parte, este efecto inhibidor no tiene por objeto eliminar otras bacterias, sino solo la prevención de un crecimiento excesivo de los microorganismos en un ecosistema integrado. La difusión de los antibióticos segregados por bacterias productoras asegura una «zona exclusiva» a una cierta distancia de estas. En los límites de esa zona, las bacterias potencialmente competidoras se enfrentan a concentraciones antibióticas muy bajas, insuficientes para eliminarlas, pero sí para reducir su tasa de crecimiento y evitar la sobrepoblación. Estos fenómenos de inhibición son frecuentemente recíprocos y multilaterales, lo que asegura la diversidad y el equilibrio del conjunto; las bacterias son profundamente demócratas, o, al menos, son un perfecto ejemplo, totalmente compatible con los enunciados de Thomas Hobbes (1588-1679), de cómo las leyes naturales, reduciendo la libertad (libertad para dominar) de cada individuo, aseguran el mantenimiento de la existencia común, y, en suma, de la existencia biológica misma. Los antibióticos son una parte de la red de señales intercelulares e interpoblacionales que mantienen la diferenciación y la diversidad en la microbiosfera (Linares et al., 2006). Actúan por tanto como moléculas-señales, como hormonas que integran el funcionamiento de sistemas complejos. Como ocurre con la mayor parte de señales, su concentración «señaladora» fisiológica es probablemente muy baja.
La producción antropogénica de antibióticos equivale a la producción de «señales» intercelulares en cantidades inimaginablemente altas, que se liberan a la microbiosfera. La alta densidad de señales debe producir un alto nivel de «ruido» indescifrable, con efectos deletéreos sobre las redes informacionales de los sistemas biológicos, cuyas consecuencias ecológicas y evolutivas estamos lejos de poder descifrar.
La lucha contra las bacterias patógenas: un problema global
Por supuesto, el peligro más inmediato y visible de la liberación al medio (incluyendo los individuos tratados) de altas cantidades de antibióticos de origen industrial es el desarrollo de microorganismos resistentes entre las poblaciones bacterianas patógenas, que pueden dar lugar a infecciones intratables. Como dijo Stuart Levy en su famoso libro The Antibiotic Paradox, el mal uso de los antibióticos por parte del hombre está causando su propia devaluación como fármacos curativos. En realidad, el problema de la resistencia a antibióticos ha llegado a un punto de no-retorno. Durante mucho tiempo –demasiado tiempo– se ha postulado que un «uso adecuado de los antibióticos» (en romance paladino: menor uso, con mejor detección de los casos en que el tratamiento es realmente necesario) debería llevar a una reducción de las resistencias. Esta sería la consecuencia de un menor efecto selectivo, y también se ha supuesto que las bacterias resistentes deberían pagar un cierto «coste biológico» para mantener esa nueva función, de forma que en ausencia de antibióticos las bacterias sensibles tendrían ventaja y acabarían por prevalecer. Es verdad que a nivel individual, de hospital o incluso de región geográfica, hay más resistencia cuantos más antibióticos se consumen. Sin embargo, la polución antibiótica global ha llevado a una verdadera invasión planetaria de bacterias resistentes. Como decía Carl Sagan en su novela Contact, «las fronteras son siempre arbitrarias, el planeta es real», y en las regiones con mejor «política de antibióticos» asistimos ya a la invasión, desde fuentes externas, de bacterias con resistencias a los antimicrobianos.

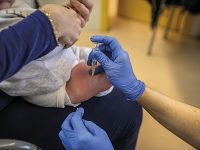
El mal uso de los antibióticos en los lugares donde existen grandes masas de población humana y animal y un medio sanitario subóptimo puede tener consecuencias a nivel global. La bacteria Staphylococcus aureus fue «humana» en China hace muchos años, pasó a los cerdos, se transmitió activamente en las granjas, se adaptó a los animales y redujo su patogenicidad para el hombre, pero en este proceso adquirió los mecanismos genéticos de resistencia a antimicrobianos. En Europa, de nuevo el clon resistente CC398 ha contaminado a humanos. / Carl Jones
Los países de Oriente, cada vez más interconectados con Occidente, poseen grandes masas de población humana y animal, un medio sanitario subóptimo con graves deficiencias en la sanidad medioambiental, y su creciente desarrollo les permite un alto grado de utilización de antimicrobianos. El resultado es un «reactor» donde la evolución de la resistencia a antimicrobianos se está precipitando. Dos ejemplos reflejan esta situación. El primero es la inesperada aparición en casos humanos en Holanda de Staphylococcus aureus con resistencia a meticilina (a todos los antibióticos beta-lactámicos). Estudios moleculares han demostrado que el clon bacteriano responsable, S. aureus CC398, llegó a Europa a través de animales (cerdos) de origen chino. Esta bacteria fue «humana» en China hace muchos años, pasó a los cerdos, se transmitió activamente en las granjas, se adaptó a los animales y redujo su patogenicidad para el hombre, pero en este proceso adquirió los mecanismos genéticos de resistencia a antimicrobianos. En Europa, de nuevo el clon resistente CC398 ha contaminado a humanos. El segundo ejemplo se relaciona con la aparición en Europa (Suecia y Reino Unido) de cepas de enterobacterias con un nuevo enzima de multiresistencia a beta-lactámicos, la Nueva Delhi metalobetalactamasa (NDM), procedente de la «importación» de un caso humano desde Nueva Delhi, en la India. Se ha demostrado de hecho que la cepa está muy diseminada en la India, donde probablemente se produjo su emergencia. En Europa ha tenido lugar una diseminación secundaria que también ha alcanzado a España.
Claves evolutivas
¿Cuáles son las claves evolutivas de la invasión planetaria de la resistencia a los antibióticos? ¿Qué podemos hacer para controlar esta situación? La primera clave evolutiva es la masiva producción industrial de fármacos antimicrobianos, su uso masivo en medicina, veterinaria y agricultura, y la liberación consecuente de estas substancias al medio ambiente. Como hemos visto, el efecto esperado es la selección de poblaciones resistentes, pero también la aceleración de la variación bacteriana y la distorsión del sistema de señales que regula la homeostasis de la microbiosfera. Sería necesario regular no solo el uso adecuado, sino la biodegradación (antibióticos biodegradables) o al menos el confinamiento y tratamiento de los residuos que contengan antibióticos.
La segunda clave evolutiva es la interacción entre las bacterias colonizadoras o patogénicas de hombres y animales con los microorganismos del medio ambiente. Las bacterias medioambientales (del suelo, en particular de la rizosfera; y del agua, en especial de los sedimentos) contienen un completísimo repertorio de genes de resistencia (el resistoma medioambiental) que pueden ser transferidos por elementos genéticos móviles a las bacterias peligrosas para la salud pública. Las bacterias de origen humano y animal (imaginemos aguas residuales de hospitales, de granjas) están pasando con pocas limitaciones al medio ambiente, contaminan los ecosistemas con genes de resistencia amplificados por acción antropogénica, y pueden a su vez recibir nuevos genes desde las bacterias medioambientales. La densidad de interacciones es enorme en países hiperpoblados con bajo nivel sanitario. Es incomprensible que los epidemiólogos y sanitarios no hayan sido capaces de proponer seriamente la absoluta necesidad de impedir el contacto entre bacterias humanas-animales y medioambientales (Baquero et al., 2008). Necesitamos tecnología de esterilización de nuestros residuos (aguas fecales) antes de ser liberados al medio, tanto a nivel industrial (por ejemplo depuradoras a la salida de los hospitales) como familiar, en regiones de bajo nivel sanitario (mini-tanques sépticos).
«El peligro más inmediato y visible de la liberación al medio de altas cantidades de antibióticos de origen industrial es el desarrollo de microorganismos resistentes entre las poblaciones bacterianas patógenas»
La tercera clave evolutiva es la diseminación global de los clones bacterianos de alto riesgo que hacen circular la resistencia a antibióticos a nivel planetario, y diseminarla a otras bacterias. Estos clones circulan probablemente por las que Mark Ragan calificó como «autopistas de la circulación de genes». La amplia circulación asegura el progresivo reclutamiento de nuevos genes y el desarrollo de bacterias multiresistentes. Debemos mejorar nuestra tecnología para detectar con técnicas rápidas estos clones de alto riesgo en los hombres, animales y medio ambiente, e identificar las «autopistas» por las que circulan en el planeta. Debemos mejorar nuestras posibilidades para eliminar dichos clones peligrosos, con una «terapéutica dirigida a clon» (clone-directed therapy) o aplicando estrategias vacunales específicas. Existen precedentes del éxito potencial de estas intervenciones, como la vacunación contra clones resistentes de Streptococcus pneumoniae o Haemophilus influenzae.
La cuarta clave evolutiva radica en que la evolución de la resistencia a los antibióticos se desarrolla en el seno de un sistema multi-jerárquico complejo. Los genes de resistencia, las plataformas genéticas en las que están situados, los elementos genéticos móviles (capaces de pasar de célula a célula) en que se insertan dichas plataformas, las células bacterianas donde entran los elementos móviles, los complejos clonales a los que pertenecen esas células, las especies y comunidades microbianas, los ecosistemas, constituyen distintas unidades evolutivas embutidas unas dentro de las otras, esto es, formando una estructura introgresiva en múltiples niveles (Bapteste et al., 2012). De hecho, habría que desarrollar una epidemiología integrada multijerárquica para poder realizar estudios de biología de poblaciones independientemente para cada unidad evolutiva, e inducir los efectos de las variaciones de los distintos elementos en el sistema complejo (Baquero et al., 2013). Conociendo estos datos, será posible en el futuro realizar una verdadera intervención eco-evo (incluyendo «fármacos» para curar de resistencia determinados ecosistemas, como el microbioma humano; Baquero et al., 2011).
En suma, la confluencia de conocimientos ecológicos y evolutivos será necesaria en el próximo futuro para comprender y corregir el importante problema de salud pública, o, si se quiere, de salud global, que constituye la exposición de la microbiosfera a cantidades masivas de antibiótico, cuyo reflejo más próximo es la resistencia a antibióticos en bacterias que infectan al hombre y a los animales.
1. El término eco-evo, acrónimo de «Ecología y Evolución», se refiere a la aproximación biológica que considera la posibilidad de estudiar y actuar integradamente en la ecología (señales ambientales) y la evolución (modificación hereditaria de los organismos como respuesta adaptativa a esas señales). (Volver al texto)
REFERENCIAS
Bapteste, E. et al., 2012. «Evolutionary Analyses of Non-genealogical Bonds Produced by Introgressive Descent». PNAS, 109(45): 18.266-18.272. DOI: <10.1073/pnas.1206541109>.
Baquero, F.; Coque, T. M. y F. de la Cruz, 2011. «Ecology and Evolution as Targets: the Need for Novel Eco-evo Drugs and Strategies to Fight Antibiotic Resistance». Antimicrob Agents Chemother, 55(8): 3.649-3.660. DOI: <10.1128/AAC.00013-11>.
Baquero, F.; Martínez, J. L. y R. Cantón, 2008. «Antibiotics and Antibiotic Resistance in Water Environments». Current Opinion in Biotechnology, 19: 260-265. DOI: <10.1016/j.copbio.2008.05.006>.
Baquero, F.; Tedim, A. P. y T. M. Coque, 2013. «Antibiotic Resistance Shaping Multilevel Population Biology of Bacteria». Frontiers in Antimicrobials, Resistance and Chemotherapy. Prepublicat online: 6 de marzo de 2013. DOI: <10.3389/ fmicb.2013.00015>.
Galán, J. C.; González-Candelas, F.; Rolain, J. M. y R. Cantón, 2013. «Antibiotics as Selectors and Accelerators of Diversity in the Mechanisms of Resistance: from the Resistome to Genetic Plasticity in the β-lactamases World». Frontiers in Antimicrobials, Resistance and Chemotherapy. Publicado online: 8 de febrer de 2013. DOI: <10.3389/fmicb.2013.00009>.
Levy, S. B., 2002. The Antibiotic Paradox. Da Capo Press. Cambridge, MA.
Linares, J. F.; Gustafsson, I.; Baquero, F. y J. L. Martínez, 2006. «Antibiotics as Intermicrobial Signaling Agents Instead of Weapons». PNAS, 103(51): 19.484-19.489. DOI: <10.1073/pnas.0608949103>.