De agricultoras a bioingenieras
Sembrando genes, cosechando moléculas

La agricultura del siglo XXI se enfrenta a grandes desafíos a los que es necesario responder de forma urgente. En la última década se han desarrollado nuevas tecnologías de mejora genética que pueden contribuir a afrontar estos retos. Estas tecnologías no son solo más precisas y eficientes, sino también más sencillas y accesibles, lo que facilitará una progresiva democratización de la biotecnología agraria. En este artículo analizamos el desarrollo de la agricultura del futuro bajo las premisas de una democratización tecnológica y una relajación regulatoria. En este escenario cabría esperar un aumento de la diversidad de variedades y especies cultivadas, un fuerte desarrollo de cultivos biofactoría y, a más largo plazo, la aparición de cultivos inteligentes con capacidades aumentadas.
Palabras clave: nuevas tecnologías de mejora, edición genética, biología sintética, plantas biofactoría.
Introducción
Los ciudadanos de los países desarrollados tendemos a considerar que el suministro de alimentos está garantizado con el nivel tecnológico actual, y subestimamos así la importancia estratégica de la biotecnología agraria (Figura 1). Sin embargo, esta postura no puede estar más alejada de la realidad. Según el último informe sobre el futuro de la agricultura de la FAO, la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO, 2018), la población crecerá hasta alcanzar los 10.000 millones de habitantes en 2050, lo que conllevará un aumento de las tierras cultivadas y un consiguiente descenso de la superficie forestal. Al mismo tiempo, el cambio climático amenaza con reducir la productividad de nuestros cultivos. Nuevas plagas ponen en riesgo nuestras plantas, favorecidas por el flujo de mercancías y por unas condiciones climáticas más apropiadas para su desarrollo. A su vez, la lucha contra estas plagas emergentes obligará a incrementar el uso de fitosanitarios, con la consiguiente generación de residuos de posible toxicidad. En este contexto de presiones demográficas y medioambientales, la mejora de nuestros sistemas de producción agrícola es imprescindible si queremos alcanzar un futuro sostenible.
«La mejora genética consiste en equipar nuestros cultivos con mecanismos genéticos propios que los defiendan de las nuevas amenazas»
Una de las estrategias más eficientes de que disponemos para enfrentar estos desafíos es la mejora genética, que consiste en equipar nuestros cultivos con mecanismos genéticos propios que los defiendan de las nuevas amenazas sin necesidad del uso de agentes externos. Ahondar en la mejora genética enfocada hacia factores de sostenibilidad, como la resistencia genética a plagas y enfermedades, resiliencia y adaptación a salinidad, sequía, altas temperaturas, etc., es uno de los mayores retos de futuro que tiene la biotecnología vegetal. Sin embargo, al igual que ocurrió en el pasado en otros ámbitos tecnológicos, el modelo de desarrollo agrobiotecnológico del futuro dependerá en gran parte de cómo las nuevas tecnologías de mejora vegetal sean percibidas por la sociedad. Repasemos como ejemplo la evolución de la informática y las telecomunicaciones. En el siglo pasado, la computación comenzó siendo una tecnología profundamente elitista monopolizada por estados y grandes empresas, que generaba desconfianza entre la población. Todo esto cambió radicalmente con la democratización que supuso la aparición del ordenador personal, que a su vez fue posible gracias al abaratamiento de la tecnología de la mano de la estandarización de los componentes electrónicos.

Figura 2. Hasta el momento la biotecnología se asocia a una tecnología elitista. No obstante, las nuevas tecnologías de mejora nos sitúan en un momento en el que es posible realizar un salto de «democratización», similar al que supuso la llegada del ordenador personal. / HCC Public Information Office
Hasta la fecha la biotecnología agraria se ha conducido también como una tecnología elitista, reflejo de lo cual es el escaso número de compañías que concentran la mayor parte de la producción de semillas en el mundo (Figura 2). Como veremos a continuación, las nuevas tecnologías de mejora, unidas al ingente corpus de conocimiento generado en las últimas décadas por disciplinas como la genómica y la fisiología vegetal, nos sitúan en una posición tecnológica que permitiría un salto de «democratización» similar al que tuvo lugar con el ordenador personal. Sin embargo, el hecho de que se den las condiciones tecnológicas idóneas no asegura que dicha transición tenga lugar. Todo dependerá de cómo la tecnología sea percibida, aceptada y eventualmente incorporada en nuestras sociedades.
La situación puede oscilar desde un escenario ultraconservador, con un rechazo frontal a las nuevas tecnologías, hasta el escenario ultraliberal que prescinde casi totalmente de cualquier regulación. Es razonable esperar que ninguno de los escenarios extremos tenga lugar, pero aun evitando las posiciones extremas, pequeñas diferencias de tratamiento de las barreras regulatorias pueden dar lugar a resultados completamente distintos. Una postura más restrictiva, basada en una aplicación rigurosa del principio de precaución, generará dificultades al desarrollo tecnológico franqueables solo por unos pocos actores con capacidad financiera suficiente para superar las barreras de desregulación. Tendremos entonces la biotecnología de unos pocos. En cambio, un escenario con una regulación más accesible podría estimular la creatividad, la competencia y favorecer la aparición de un número mayor de actores, incluyendo aquellos que actúan en áreas rurales, sin afectar por ello a la seguridad alimentaria o medioambiental.
A continuación, examinaremos cuál puede ser el paisaje agroalimentario del futuro suponiendo el escenario más favorable para una innovación responsable. Para ello, en primer lugar, analizaremos de qué forma algunas de las nuevas tecnologías facilitadoras han colocado la mejora genética agraria en el punto de inflexión en el que se encuentra en la actualidad, para después imaginar de qué forma estas tecnologías, en un contexto favorable para la innovación, darían lugar a las plantas del futuro.
Nuevas herramientas de mejora
La mejora genética consiste en modificar algunas de las instrucciones genéticas contenidas en el genoma de una especie para adaptarla a nuestras necesidades. Los humanos llevamos modificando el genoma de nuestros cultivos desde el Neolítico, al haber ido seleccionando aquellas mutaciones que por azar resultan más beneficiosas. Sin embargo, hasta el siglo pasado nuestra capacidad de generar cambios genéticos estaba limitada a la aparición de mutaciones espontáneas. Más recientemente, la mejora asistida por marcadores ha permitido acelerar la incorporación a nuestros cultivos de mutaciones provenientes de genomas de otras variedades o especies relacionadas.
«Aún hoy, muchos de los medicamentos usados en la lucha contra enfermedades como el cáncer o la malaria son extraídos de las plantas»
Por su parte, las técnicas de mutagénesis química y por radiación han facilitado la rápida generación de nueva variabilidad genética para incorporarla a los programas de mejora. Sin embargo, no fue hasta principios de los ochenta cuando la transformación genética vegetal permitió por primera vez transferir instrucciones «de diseño», es decir, no generadas al azar, al genoma de una planta (Barton, Binns, Matzke y Chilton, 1983; Herrera-Estrella, Depicker, Van Montagu y Schell, 1983). Nótese que las plantas transgénicas que se cultivan en la actualidad incorporan normalmente solo uno o a lo sumo unos pocos genes «de diseño» resultantes de la recombinación de DNA. Una minucia comparada con los cerca de 50.000 genes que conforman el genoma de una planta como la soja (Schmutz et al., 2010). Y pese a ello, el impacto de la transformación genética de plantas ha sido tal que el 75 % de la soja que se planta hoy en día es portadora de esas pocas modificaciones genéticas.

Figura 3. En los próximos diez años se espera una explosión de diversidad, tanto de variedades (gracias a la mejora de variedades locales) como de especies cultivadas. / PxHere
Frente a esta primera generación de herramientas biotecnológicas, en la última década nuestras capacidades de intervenir en los genomas han aumentado de forma radical gracias a un conjunto de nuevas tecnologías entre las que destacaré dos: la síntesis de DNA y la edición genética CRISPR. La síntesis de DNA nos permite escribir instrucciones genéticas en un tubo de ensayo. En los últimos años nuestra capacidad de síntesis ha crecido casi exponencialmente y cada vez somos capaces de escribir fragmentos de DNA más largos con menor coste (Wang et al., 2018). Aunque la longitud de las cadenas de DNA que se pueden sintetizar de una sola vez mediante métodos puramente químicos no es ilimitada, recientemente las llamadas «técnicas de ensamblaje modular» han permitido crear construcciones cada vez más largas uniendo fragmentos de DNA entre sí como si de piezas de Lego se tratara (Engler, Kandzia y Marillonnet, 2008; Vazquez-Vilar, Orzaez y Patron, 2018). Como consecuencia, nuestra capacidad de «escribir» instrucciones complejas que puedan ser posteriormente transferidas a la planta ha crecido enormemente, no solo en cantidad sino también en precisión, al tiempo que se ha reducido el precio y el esfuerzo que cuesta generarlas.
El segundo gran avance tecnológico a destacar está siendo la tecnología CRISPR de edición genética. De poco sirve escribir instrucciones genéticas si no podemos insertarlas en la página correcta dentro del correspondiente libro de instrucciones. Las proteínas CRISPR/Cas9, descubiertas entre otros por el ilicitano Francis Mojica (Lander, 2016; Mojica, Díez-Villaseñor, García-Martínez y Almendros, 2009), son el equivalente en el genoma a potentes programas de búsqueda, que nos permiten orientarnos en el inmenso libro de instrucciones del genoma y, bien introducir pequeñas modificaciones, o bien incorporar con precisión nueva información. Lo novedoso de la tecnología CRISPR es que podemos incorporar la nueva información exactamente en el renglón elegido de la página deseada, allá donde una instrucción tenga su sentido y en ningún otro lugar. Es importante destacar que la edición genética CRISPR ha resultado una tecnología no solo enormemente eficiente sino también muy asequible, lo que pone toda su potencia al alcance de pequeños laboratorios. Es también fácil inferir que la combinación de una creciente capacidad de síntesis de DNA, con la potencia y la precisión que permiten la edición genómica, puede colocar a la mejora genética en el punto de partida de una revolución tecnológica.
De agricultoras a bioingenieras
A continuación, examinaremos cómo pueden ser las plantas del futuro habida cuenta de nuestras nuevas capacidades tecnológicas. Como se ha descrito anteriormente, asumiremos un escenario de regulación lo suficientemente flexible para no hacer inviable su adopción por parte de pequeñas y medianas empresas o sus equivalentes en el ámbito público. Una primera consecuencia de un escenario así sería la creación de un nuevo ecosistema de innovación asociado a la agricultura. Uno de los principales problemas del sistema actual es la tendencia a la uniformidad en el desarrollo de variedades élite que sustituyen a las variedades autóctonas. La «democratización» de la agrobiotecnología facilitaría la introducción de innovaciones genéticas tales como resistencias, calidades organolépticas o nutricionales, etc., directamente sobre las variedades locales. De esta forma se acercaría el diseño genético al productor local. En otras palabras, la «democratización» de la biotecnología permitiría el tránsito profesional de agricultoras a «agricultoras-bioingenieras», o incluso «biohackers», profesionales especializadas en distintas fases del ciclo productivo agrícola, desde el diseño de la variedad hasta su producción en campo. En este ambiente abonado a la creatividad es donde las plantas del futuro nos pueden dar agradables sorpresas. A continuación, exploramos algunos ejemplos de cómo podría ser esta nueva agricultura creativa.
Explosión de la biodiversidad cultivada
El cambio más inmediato que cabría esperar en un horizonte de diez años es una explosión de diversidad, tanto de variedades como de especies (Figura 3). En primer lugar, se ampliaría la diversidad varietal, fruto de la facilitación de la mejora en variedades locales. Más a medio plazo, cabría también esperar un aumento del número de especies cultivadas. En agricultura utilizamos solo una parte ínfima del catálogo de especies vegetales que existen en la naturaleza, ya que son pocas las que se dejan domesticar mediante métodos tradicionales. Sin embargo, hoy conocemos muchos de los factores genéticos que han permitido la domesticación de nuestras plantas de cosecha, y ayudados por las nuevas técnicas de mejora, se hace posible emprender la domesticación de nuevas especies silvestres. Así, en un reciente ejemplo, un grupo de investigadores alemanes y brasileños consiguieron mejorar una especie de tomate silvestre sin valor agronómico mediante la edición génica de seis de sus genes: multiplicaron por diez el número de frutos por planta, triplicaron el tamaño y quintuplicaron el contenido en licopeno (Khan, Zaidi, Amin y Mansoor, 2019; Zsögön et al., 2018). En cierta forma estos investigadores recapitularon en un par de generaciones buena parte del proceso centenario de domesticación del tomate cultivado.
«Los humanos llevamos modificando el genoma de nuestros cultivos desde el Neolítico»
Es de esperar que procesos similares se produzcan en otras especies silvestres o semidomesticadas, muchas de las cuales pueden aportar mayor resiliencia de base, o mejor adaptación a ambientes hostiles. Las nuevas tecnologías nos permiten incluso acelerar los procesos de especiación, como demostró recientemente el grupo del profesor Ralf Bock en Alemania mediante la neopoliploidización inducida por injerto (Fuentes, Stegemann, Golczyk, Karcher y Bock, 2014). Partiendo de dos especies de tabaco, Nicotiana tabacum y Nicotiana glauca, estos investigadores crearon de forma acelerada una nueva especie (Nicotiana tabauca), resultado de la transferencia de genomas nucleares completos de una planta a otra. Tras la transferencia, se produce un rápido proceso de reorganización genómica similar al que ocurre durante la especiación natural. De esta manera se pueden generar rápidamente nuevas especies sobre las que ensayar sus características agronómicas, su composición, etc., y crear así cultivos radicalmente nuevos.

Figura 4. La especie Nicotiana benthamiana, conocida cariñosamente como Benthy, se utiliza ampliamente para producir vacunas, anticuerpos y nuevos productos que sustituyan a los antibióticos. La ingeniería genética nos permite utilizar las plantas como biofactorías de biomoléculas usadas en farmacia, medicina o cosmética. / CSIC-CRAG
Cultivos de biomoléculas: “made in benthy”
El ejemplo anterior sirve para subrayar el hecho de que, además de para la producción de alimentos, existe una tradición milenaria del uso de las plantas como factorías de compuestos de utilidad, desde fibras y biomateriales hasta medicamentos. Aún hoy, muchos de los medicamentos usados en la primera línea de lucha frente a enfermedades como el cáncer o la malaria son extraídos de las plantas. La ingeniería genética nos permite utilizar las plantas como biofactorías de biomoléculas usadas en farmacia, medicina o cosmética. Así, la especie australiana Nicotiana benthamiana (Figura 4), un pariente enano del tabaco (conocido cariñosamente como Benthy), se utiliza ampliamente para producir vacunas, anticuerpos y nuevos productos que sustituyan a los antibióticos. El antídoto administrado a los misioneros occidentales en la reciente crisis de ébola de 2014 fue producido en N. benthamiana (Qiu et al., 2014).
Más recientemente, la empresa canadiense Medicago acaba de finalizar la fase III de sus pruebas clínicas en humanos de una vacuna para la gripe estacional, también «made in benthy» (Pillet et al., 2016). Es muy probable que en un horizonte de cinco a diez años nos vacunemos con antígenos producidos en plantas, y que nuestros alimentos se conserven con colicinas (proteínas antibacterianas), «made in benthy», como las que ha desarrollado recientemente la empresa alemana Icon Genetics (Stephan et al., 2017). Todos estos ejemplos muestran una nueva vertiente de la producción agrícola, que a su vez plantea nuevos objetivos de mejora genética hasta ahora inexplorados, como el rendimiento, la calidad y estabilidad de las proteínas recombinantes o la bioseguridad de los cultivos, entre otros. El proyecto europeo Newcotiana,1 que reúne a diecinueve grupos de investigación europeos y australianos, busca precisamente mejorar la capacidad como biofactorías de las plantas de Benthy y su pariente el tabaco cultivado. Con la implementación de estas mejoras es de esperar que en el futuro aumente la superficie dedicada a plantas biofactorías, y que estas desplacen a otros cultivos socialmente menos aceptables, como el tabaco de fumar.
Plantas «sexis», «inteligentes» y con capacidades aumentadas
¿Qué podemos esperar en un horizonte más allá de veinte años? ¿Cuáles son los límites de la mejora genética? ¿Podemos equipar a nuestros cultivos con nuevas funcionalidades, más allá de las que observamos en la naturaleza? Hay quien dirá que ya todo está inventado por la evolución, pero bien mirado resulta obvio que los humanos podemos aportar capacidades de las que la evolución biológica no ha dispuesto en ningún caso. Un ejemplo es la predicción meteorológica. Resulta tecnológicamente plausible diseñar plantas «inteligentes» capacitadas para responder con antelación a una alerta meteorológica, como por ejemplo una helada, con la producción de compuestos defensivos como una proteína anticongelante. Igualmente, el estado actual de la tecnología permitiría diseñar plantas que, ante la detección remota de una plaga, respondan con la producción de compuestos volátiles defensivos, como feromonas sexuales que confundan a los insectos.
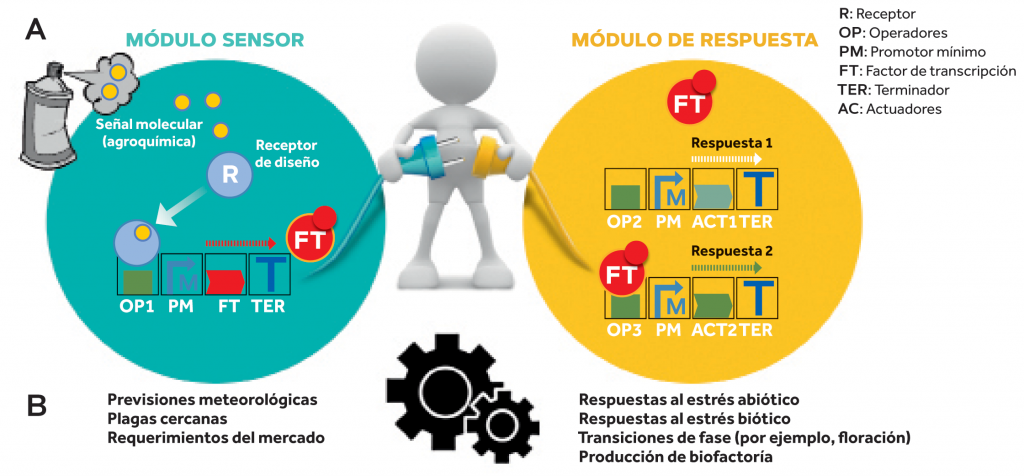
Figura 5. Este esquema muestra cómo se equipa de nuevos circuitos genéticos a las plantas para convertirlas en «inteligentes». (A) Los principios de modularidad y estandarización propios de la biología sintética facilitan la conexión física entre elementos genéticos y por tanto la construcción de circuitos cada vez más complejos de regulación. (B) Aplicados a la mejora genética, esos circuitos permitirían conectar señales operadas externamente con circuitos de regulación endógenos como aquellos que gobiernan las respuestas al estrés, los cambios de fase, etc.
Los ejemplos que hemos citado implican equipar a las plantas no con un solo transgén o una pequeña modificación, sino con circuitos genéticos y rutas metabólicas complejas que implican muchos genes. Algunos autores defienden que, para alcanzar los niveles de sofisticación requeridos para diseñar este tipo de plantas, es necesario incorporar a la biotecnología principios ingenieriles similares a los que permitieron despegar a la revolución industrial y más tarde a las ingenierías de la información, como la estandarización, la modularidad o la abstracción de función. Estos aspectos los aborda la disciplina conocida como biología sintética, y suponen un nuevo horizonte para la biotecnología vegetal. El ejemplo de las plantas que producen feromonas sexuales fue inicialmente planteado e implementado parcialmente por un equipo de estudiantes de la Universidad Politécnica de Valencia en colaboración con el CSIC en el contexto del proyecto iGEM de Biología Sintética celebrado en Boston en 2014, y fue la semilla de otros proyectos de investigación que siguen la misma línea de desarrollo, es decir, la bioproducción sostenible de feromonas de insectos en plantas como alternativa al uso de plaguicidas de síntesis.
«Hoy conocemos muchos de los factores genéticos que han permitido la domesticación de nuestras plantas de cosecha»
Por su parte, el ejemplo de la respuesta a predicciones meteorológicas viene a ilustrar la potencialidad del diseño de circuitos genéticos que permitan operar externamente procesos endógenos de interés agronómico, como el tiempo de floración, la activación de mecanismos de defensa o protección frente a estreses ambientales (Figura 5). De forma similar a como la realidad aumentada o la interfaz «cíborg» con elementos cibernéticos permiten a los humanos ir más allá de nuestras capacidades innatas en el conocimiento del medio exterior, la biología sintética busca crear plantas de cosecha con capacidades aumentadas, que les permitan producir más con menos, de forma sostenible y respetuosa con el medio ambiente.
Los desafíos son enormes, pero en los ecosistemas de conocimiento donde se combina el fomento de la creatividad con el incentivo de la necesidad casi ningún reto tecnológico es infranqueable. Las plantas del futuro serán probablemente como nosotros queramos que sean. Las decisiones empiezan a tomarse hoy mismo, y de nuestras decisiones presentes dependerá el futuro de las siguientes generaciones sobre la Tierra.
Notas
1. <https://newcotiana.org/> (Volver al texto)
Referencias
Barton, K. A., Binns, A. N., Matzke, A. J., & Chilton, M. D. (1983). Regeneration of intact tobacco plants containing full length copies of genetically engineered T-DNA, and transmission of T-DNA to R1 progeny. Cell, 32(4), 1033–1043. doi: 10.1016/0092-8674(83)90288-x
Engler, C., Kandzia, R., & Marillonnet, S. (2008). A one pot, one step, precision cloning method with high throughput capability. PLOS ONE, 3(11), e3647. doi: 10.1371/journal.pone.0003647
FAO. (2018). The future of food and agriculture: Alternative pathways to 2050. Roma: Food and Agriculture Organitzation of the United Nations. Consultat en http://www.fao.org/3/I8429EN/i8429en.pdf
Fuentes, I., Stegemann, S., Golczyk, H., Karcher, D., & Bock, R. (2014). Horizontal genome transfer as an asexual path to the formation of new species. Nature, 511(7508), 232–235. doi: 10.1038/nature13291
Herrera-Estrella, L., Depicker, A., Van Montagu, M., & Schell, J. (1992). Expression of chimaeric genes transferred into plant cells using a Ti-plasmid-derived vector. Nature, 303, 209–213. doi: 10.1038/303209a0
Khan, M. Z., Zaidi, S. S., Amin, I., & Mansoor, S. (2019). A CRISPR way for fast-forward crop domestication. Trends in Plant Science, 24(4), 293–296. doi: 10.1016/j.tplants.2019.01.011
Lander, E. S. (2016). The heroes of CRISPR. Cell, 164(1-2), 18–28. doi: 10.1016/j.cell.2015.12.041
Mojica, F. J., Díez-Villaseñor, C., García-Martínez, J., & Almendros, C. (2009). Short motif sequences determine the targets of the prokaryotic CRISPR defence system. Microbiology, 155(3), 733–740. doi: 10.1099/mic.0.023960-0
Pillet, S., Aubin, E., Trépanier, S., Bussière, D., Dargis, M., Poulin, J. F., … Landry, N. (2016). A plant-derived quadrivalent virus like particle influenza vaccine induces cross-reactive antibody and T cell response in healthy adults. Clinical Immunology, 168, 72–87. doi: 10.1016/j.clim.2016.03.008
Qiu, X., Wong, G., Audet, J., Bello, A., Fernando, L., Alimonti, J. B., … Kobinger, G. P. (2014). Reversion of advanced Ebola virus disease in nonhuman primates with ZMapp. Nature, 514(7520), 47–53. doi: 10.1038/nature13777
Schmutz, J., Cannon, S. B., Schlueter, J., Ma, J., Mitros, T., Nelson, W., … Jackson, S. A. (2010). Genome sequence of the palaeopolyploid soybean. Nature, 463, 178–183. doi: 10.1038/nature08670
Stephan, A., Hahn-Löbmann, S., Rosche, F., Buchholz, M., Giritch, A., & Gleba, Y. (2017). Simple purification of Nicotiana benthamiana-produced recombinant colicins: High-yield recovery of purified proteins with minimum alkaloid content supports the suitability of the host for manufacturing food additives. International Journal of Molecular Sciences, 19(1), 95. doi: 10.3390/ijms19010095
Vazquez-Vilar, M., Orzaez, D., & Patron, N. (2018). DNA assembly standards: Setting the low-level programming code for plant biotechnology. Plant Science, 273, 33–41. doi: 10.1016/j.plantsci.2018.02.024
Wang, L., Jiang, S., Chen, C., He, W., Wu, X., Wang, F., … Chen, S. (2018). Synthetic genomics: From DNA synthesis to genome design. Angewandte Chemie International Edition English, 57(7), 1748–1756. doi: 10.1002/anie.201708741
Zsögön, A., Cermák, T., Naves, E. R., Notini, M. M., Edel, K. H., Weinl, S., … Peres, L. E. P. (2018). De novo domestication of wild tomato using genome editing. Nature Biotechnology, 36, 1211–1216. doi: 10.1038/nbt.4272





